الودگی خاک با مواد رادیواکتیو و مکانیزم های کنترل آن
- Hits: 4733

گرد آوری و تدوین:دکتر سلطانی نژاد
آلودگی خاک با مواد رادیواکتیو و مکانیزم های کنترل آن


آلودگی خاک با عناصر رادیو اکتیو و نحوه درمان خاک:
پیشگفتار:
ایزوتوپهای رادیو اکتیو بعضی از فلزات و شبه آنها بصورت طبیعی و همچنین در نتیجه فعالیت های انسانی در سیستم های خاک بوجود می آیند.
حرکت عناصر فوق و زیست دستیابی (میزان و مقدار مواد رادیو اکتیو در بدنه محیط زیست یعنی اب ،خاک، گیاهان،جانوران و انسانbioavailability )آنها در سیستم های زنده مسئله ئی در خور توجه است که باید در مورد آن تحقیقات گسترده ئی صورت گیرد.
این مهم در خصوص فلزات رادیواکتیو و غیر رادیواکتیو صادق است.
در این مقاله کوشش می شود تا بعضی از فلزات رادیواکتیو که باعث آلودگی خاک می گردند، مورد بررسی قرار گیرند.
تفاوت های مهمی وجود دارد که می شود فلزات رادیواکتیو را بصورت جداگانه در خاک درمان و تصحیح نمود.
قبل از پرداختن به موضوع اصلی بحث توضیح نکات ذیل ضروری است:
1- ایزوتوپهای رادیواکتیو بعضی از فلزات علاوه بر اثرات بیولوژیکی، قادرند با سایر ایزوتوپهای همان عنصر فلزی مشارکت داشته و در چنین حالتی ممکن است به علت اشعه هائی که ساطع می کنند، اثرات نامطلوبی به بار آورند.
2- ایزوتوپهای رادیواکتیوفلزی علاوه بر نقش پیچیده ئی که در تعیین جابجائی فلزات در خاک دارند،نیز قادرند بر موجودات زنده موجود در خاک اثر گذاشته و واکنش های فیزیکی تشعشع با خاک باعث می گردد که اشعه های بالقوه ی یونیزه ی مخرب موجودات زنده تولید گردد.
3- نقطه مهمی که وجود دارد تحقیقات ناکافی و بسیارناجیزی در خصوص ویژه گیهای بالقوه سمی رادیواکتیو در خاک صورت گرفته است.
4- نهایتاً اینکه آستانه غلظت مجاز این گونه فلزات و اثرات بیولوژیکی نامطلوب تشعشع، مقوله بسیار مهمی است که باید مورد کنکاش جدی قرار گیرد.
هدف اصلی و اساسی این مقاله به تصویر کشیدن شباهت ها و تفاوت ها بین رفتار رادیو نیوکلید های فلزی و سایر فلزات در سیستم های خاک است.
در این مقاله تلاش میشود، بعضی از اصول اساسی ، که نشان دهنده خطرات مترتب بر رادیونیوکلیدها (radionuclides) است ، در سیستمهای خاک بررسی گردد.
البته تکیه اصلی بر فلزاتی خواهد بود که مطالعات گسترده تری روی آنها صورت گرفته است.
مفاهیم فیزیکی و بیولوژیکی اساسی مربوط به طبیعت مواد رادیواکتیو و واکنشهای آنها با مواد:
واقعیت این است که تشعشع یک پدیده طبیعی است و در حقیقت تشعشع رادیواکتیو در سال 1896 میلادی توسط پروفسور هنری بیکیورل (Henri Becquerel) کشف گردید.
مکانیزم ساطع شدن اشعه بدین صورت است که هسته بعضی از اتمها که ناپایدار می باشند بنحو خود انگیخته ئیspontaneously متلاشی (واپاشی) شده و برای اینکه به یک حالت مطلوب که دارای انرژی بیشتری است برسند، از خود اشعه یونیزه ساطع می کنند.
رادیو ایزوتوپها بواسطه طبیعت تشعشعی که ساطع می کنند، انرژی و نیمه عمرشان مشخص و شناسائی می شود.
نیمه عمر عبارت است از:
زمان مورد نیاز برای واپاشی (تجزیه شدن) یک ماده رادیواکتیو به نصف میزان اولیه و بدین ترتیب کاهش میزان تشعشع از ماده با فاکتور دو است.
واحد شاخص استاندارد (SI) رادیواکتیوته، بیکیورل (Bq) نام دارد و بدین معنی است که یک واحد تلاشی و تجزیه در ثانیه است.
البته این احتمال وجود دارد که تشعشع متشکل از ذرات ، ناشی از الکترومغناطیس نیز باشد.(electromagnetic)
طبیعت فیزیکی تشعشع و انرژی آن تعیین کننده چگونگی واکنش یک ماده را نشان میدهد.
طبقه بندی ذرات ناشی از تشعشع:
الف- ذرات آلفا (Alpha particles)
متشکل از هسته های هلیم بوده و دارای شارژ (+2) و جرم (چهار واحد اتمی) هستند.
این ذرات به شکل بسیار محکمی با ماده وارد واکنش شده و براحتی متوقف می گردند.
یعنی با یک صفحه کاغذ یا یک لایه اپید رمی پوست موجودات زنده متوقف می شوند.
ولی این ذرات بنحو بسیار شدیدی قابلیت یونیدن (یونیزه شدن) داشته و بدین ترتیب هنگامیکه در تماس مستقیم با سیستمهای بیولوژیک قرار گیرند، قادرند خسارت های گسترده و قابل ملاحظه ئی به بار آورند.
بر اساس جدول تناوبی عناصر، فقط عناصر سنگین تر که غالباً اکتیندها (Actinides) هستند، ذرات آلفا را تابش می دهند.
ب- تابش های بتا (Beta radiation)
اساساً جریان یا مجموعه ئی از الکترون ها (β-) یا پوزیتورنها (+β) توسط متلاشی شدن یک نوترون یا یک پروتون در بین هسته، تشکیل می گردند.
بنابر این امر، تابش با مقداری جرم شارژ (پر) می شود. این تابش نسبت به تابش اشعه آلفا از یونیزاسیون کمتری برخوردار است.
موانع فیزیکی مورد نیاز برای توقف این اشعه بستگی به انرژی تابشی است که خود تابع ایزوتوپ می باشد.
بعنوان مثال:
اشعه بتا (β) 137CS از انرژی 0.512 و 1.17 MeV برخوردار است.
بنابراین می شود آنرا با یک شیشه 2.1 میلی متری متوقف نمود.
در صورتیکه اشعهTc99 انرژی کمتری دارد (تقریباً 0.3 MeV ) و توسط یک شیشه 0.3 میلی متری بصورت کامل متوقف می گردد.
ج- اشعه گاما (Gammma radiation)
این اشعه ممکن است به تنهائی یا همراه با اشعه بتا (Beta radiation) ساطع گردد.
گاما صرفاً الکترومغناطیسی (electromagnetic) بوده و هرگز بواسطه واکنش با مواد بصورت کامل متوقف نمی گردد.
لذا ضخامت شئی مورد نیاز (شیشه) برای کاهش آن (Υ) بستگی به دانسیته گاما (density) و انرژی تابش دارد.
برای این مهم اشعه گامای Cs137 (0.662) (MeV) با فاکتور (2.4*10)سانتی متری سرب یا 7.2 سانتی متری استیل تضعیف میگردد .
در صورتیکه برای تابش اشعه سرب (210pb)(0.013 و 0.047MeV) یک سیلندرکمتر از 0.1 سانتی متری از همان مواد (سرب)برای کاهش اشعه نیاز است.
پیامدهای بیولوژیکی تابش به مقدار (dose) اشعه دریافت شده بستگی دارد.
اشعه جذب سطحی شده یا دوز فیزیکی، مقدار و میزان انرژی انتقال یافته به ماده است.
واحد آن گریgray (Gy) بوده که ژول بر کیلوگرم است.(Jkg-1) (biological dose)
دوز بیولوژیکی یا مقدار معادل آن با واحد میلی سی ورت(Sievert) یعنی Sv بیان می شود. که عاملی کیفیتی است و بستگی به تخریب بیولوژیکی که تابش ایجاد می کند، دارد.
بدین ترتیب مقدار زیادی اشعه لازم است تا یک انسان را بسرعت از پا در بیاورد.
لذا مرگ و نابودی بستگی به مقدار تابش دریافت شده دارد.
معمولاً پراکنش تابش های زیاد بواسطه حوداث ایجاد می شود و اساساً ربطی به محیط معمولی زندگی ندارد.
دوزهای پائین (زیر یک) منجر به افزایش ریسک سرطان بوده و محتملاً این نوع سرطان نیز بستگی به میزان دوز دریافتی دارد.
مباحثات و جدلهای مداوم در خصوص اثر مقدار ناچیز دریافت پرتو وجود دارد. و در نبود اطلاعات عینی معمولاً فرض بر این است که ارتباطی خطی بین مرگ و میرهای سرطانی و دوز وجود دارد.
در دوزهای خیلی پائین که مشابه دوزهای موجود در محیط طبیعی می باشند ارتباط آشکاری بین ریسک سرطان و دوز دریافت شده وجود ندارد.
بنابراین کاهش پرتوگیری ضرورتی انکار ناپذیر است و باید تا حد ممکن از آن جلوگیری بعمل آید.
دو مسیر ممکن برای پرتوگیری وجود دارد:
1- داخلی که بعد از جذب یک منبع رادیواکتیو توسط یک موجود زنده حادث می گردد و غالباً از راه زنجیره غذائی یا اشکال دیگر آلودگی وارد بدن موجودات زنده می شود.
2- پرتوگیری خارجی که بواسطه طبیعت نفوذپذیرشدن اشعه بوجود می آید.
ورود این چنین اشعه ئی در بدن موجودات زنده پیامدهای بسیار مهمی دارد.
لذا، برای درمان سرزمین های آلوده به این نوع اشعه و محافظت از زمین های کشاورزی باید اقدامات پیشگیرانه مدنظر قرار گیرد.
برای مثال:
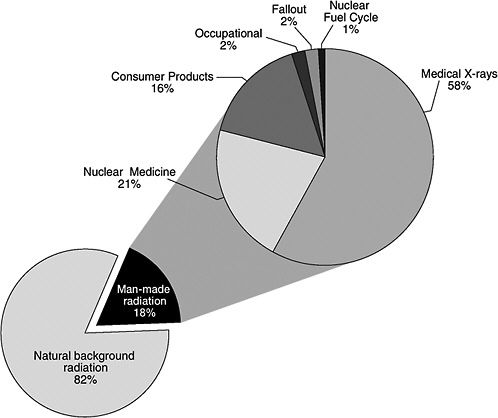
تابش های کیهانی به میزان 0.25 میلی سی ورت یا 10 درصد اشعه دریافت شده هستند و تابش های با منشاء زمینی به میزان 3/1 میلی سی ورت گزارش شده اند که این مقدار ممکن است در مناطقی که غلظت رادون بالا باشد 2 برابر است.
پرتوهای تابشی از رادیو داروها دقیقاً 0.3 میلی سی ورت در کشورهای در حال توسعه گزارش شده است.
دوز دریافت شده در کارگران بالغ در یک نیروگاه هسته ائی تقریباً در حدود 1.1 میلی سی ورت است، در صورتیکه ماکسیمم میزان مجاز 20 میلی سی ورت می باشد.
مقدار متوسط اشعه رادیواکتیو که از حادثه چرنوبیل در کشورهای مختلف اروپا حادث گردید بین 0.006 و 0.5 میلی سی ورت گزارش شده است.

منشاء فلزات رادیواکتیو در خاک:
رادیو ایزوتوپهای بعضی از فلزات بصورت طبیعی در خاک وجود دارند و معمول ترین آنها پتاسیم 40 است که دارای فراوانی طبیعی 0.012 در سطح است. و نیمه عمر آن 109X1.28 سال می باشد.
از آنجائیکه پتاسیم یک ماده مغذی اساسی بشمار می رود میانگین محتوای K40 در بدن انسان 4000bq است.
به همین ترتیب فلز قلیائی دیگر موجود در زمین روبیدیم (rubidium) است که رادیو ایزوتوپ طبیعی دارد.
87Rb دارای نیمه عمر 4.75 X 1010 سال است و مقدار آن در بدن انسان تقربیاً 600 بی کیو (Bq) می باشد.
به همین ترتیب رادیونئوکلیدهای طبیعی دیگر مانند U238 و Tu232 ، ممکن است توضیح و فراوانی نسبی آنها بواسطه معدن کاوی و سایر فعالیت های انسانی دچار تغییر گردد، و احتمال اینکه مقدار تشعشع آنها افزایش یابد نیز وجود دارد.
پراکنش مواد رادیواکتیو ناشی از آزمایش جنگ افزارهای هسته ئی در فضا در دهه های 1950 و 1960 میلادی تعداد قابل ملاحظه ئی از عنصر رادیو سی زیم (radiocesium) (137Cs و Cs134) بانیمه عمر 30.6 سال ،در محیط باعث گردید .
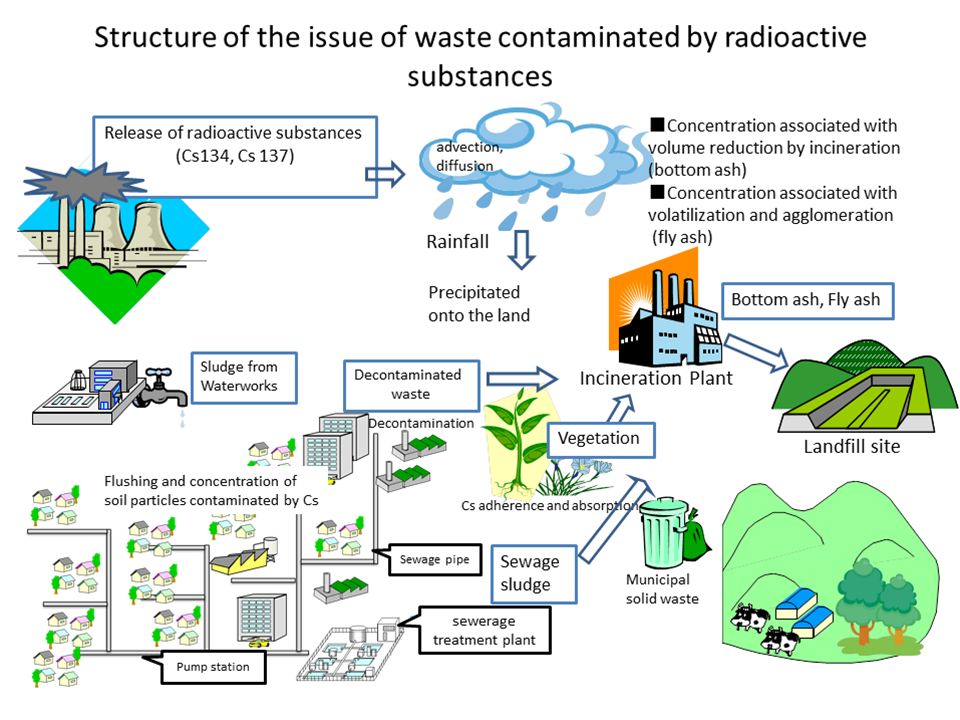
سی زیم 134-137 دارای نیمه عمر 2.134 سال در خاک و آبهای نیم کره شمالی بواسطه آزمایشات هسته ئی نیز بوجود آمده است.
تقریباً 50 سال بعدتر مقادیر ناچیزی از ایزوتوپها با عمر کوتاه از نیم کره فوق از بین رفته است.
حوادث هسته ئی و تخلیه پرتوهای ناشی از نیروگاه های هسته ئی پزشکی نیز مقادیر مختلفی از اشعه ها و سایر رادیو ایزوتوپها را در محیط زیست جاری می سازند که خطرناکترین آنها در مکانی نزدیک چرنوبیل که بواسطه انفجار هسته ئی در سال 1986 بود و باعث شد مقادیر فراوانی رادیواکتیو در آب، خاک و فضای اطراف نیروگاه پراکنده شود.
در واقع مخلوطی از رادیوایزوتوپها که غالباً فلزات بودند بواسطه انفجار نیروگاه چرنوبیل در محیط زیست پراکنده گردید.
در این انفجار عناصر سنگین تر که در شکل ذرات رها می شد در منطقه نزدیک نیروگاه هسته ئی ترسیبشده است.
سایر عناصر سبکتر از قبیل Cs، Sr و ید به مناطق دورتر در فضا پراکنده شده و همراه با نزولات جوی در غرب و شمال اروپا رسوب نمود.
تخمین های مربوط به میزان رسوب متغیر است.
این موضوع تا حدود زیادی بخاطر آن است که رسوبات، طبیعت چندگانه ئی دارند که منجر به خطای نمونه گیری می گردد.
بعلاوه بعضی از مناطق آلوده مثل پمبریا در بریتانیا قبلاً بواسطه رهاسازی انفجار سلافیل و رهاشدن سایر رادیواکتیو از منابع دیگر قبلاً آلوده گشته اند.(Baker-Cawse 1990
اگر چه اثر ( Signature) ایزوتوپی ذرات مختلف رها شده می تواند برای محاسبه منشاء آلاینده های اندازه گیری شده مورد استفاده قرار گیرد ولی این اندازه گیری بصورت اجتناب ناپذیر منجر به عدم قطعیت هائی می گردد.(uncertainties )
منشاء دیگری از رادیو نئوکلیدها که در واقع در آینده منجر به افزایش آنها می گردد ، اساساً ناشی از انبار کردن زباله های هسته ئی در محیط زیست است.
زباله های هسته ئی بر اساس فعالیت و نیمه عمر ایزوتوپهای که در آنها وجود دارد دسته بندی می گردند.
ایزوتوپهای کاملاً فعال و دارای عمر بسیار بلند که غالباً اشعه آلفا تولید می کنند و بعضاً در ضایعات هسته ئی وجود دارند.
باید بصورت بسیار مطمئن برای مدتهای بسیار طولانی در مکانهای کاملاً ایمن انبار شوند.
در حال حاضر هیچ کشوری محل ها و مکان های دائمی برای این چنین ضایعاتی در نظر نگرفته است.
مگر اینکه در آینده تحقیقاتی صورت گرفته و با امکان سنجی مکانهائی برای انبار کردن دائمی این مواد چاره اندیشی شود.
البته در گذشته این ضایعات بسیار مخرب محیط زیست در مکانهای در عمق دریا رها می گردید.
ولی در حال حاضر این گونه مکانها برای انبار کردن بدلیل خطرات محیط زیستی گسترده ،ممنوع گردیده است.
فعلاً این ضایعات خطرناک هسته ئی در مناطق عمیق خاک انبار می گردد. که در آینده می تواند خطرات گسترده ئی برای آبهای زیرزمینی و نفوذ به سطح ایجاد نمایند.
در واقع شرایط در بستر کردن (Confinement) این ضایعات و ضخامت لایه های جیولوژیکی از قبیل گل، گرانیت و نمک همراه تخریب مواد رادیواکتیو برای محدود کردن حرکت رادیوایزوتوپها ، در بیوسفور طراحی می شود.
در هر صورت سناریوهای مختلفی که می تواند منجر به آلودگی شود باید مورد بررسی و ارزیابی ریسک قرار گیرد.
بعلاوه مواد ضایعاتی رادیواکتیوی که دارای فعالیت کمتری هستند باید در سطح یا عمق انبارهای زمینی تا زمان پیدا کردن محل دفن دائمی نگه داشته شود.
به غیر از حوادث هسته ئی، رادیوایزوتوپهائی نیز وجود دارد که در ضایعات هسته ئی پیدا می شوند.
این رادیو ایزوتوپها عبارتند از:
41Ca 59,63Ni, 79Se, 90Sr, 90Y, 93Zr, 93Nb, 93Mo, 93Nb, 94Nb, 99Tc, 109mAg, 107Pd, 113mCd, 125Sb, 125mTe, 126Sn, 126Sb, 135.137Cs, 205Pb
و سایر اکتینید ها شامل اورانیوم، نپتونیوم، امریسیم و پولتونیوم نیز وجود دارند.
این مواد نه فقط از طریق نیروگاه های هسته ئی بلکه از صنایع دیگر و از رادیو داروها و تحقیقات هسته ئی نیز در آب ، خاک و هوا پراکنده می شوند.
ویژه گیهای بیولوژیکی ، فیزیکی -شیمیائی ایزوتوپهای فوق به مقدار کمی از سایر ایزوتوپهای پایدارشان متفاوت است.
در یک حالت خوش بینانه بسیار خوب، همه ایزوتوپهای یک عنصر معین، رفتار معین و مشخصی از خود نشان می دهند.
اثرات ایزوتوپی غالباً منشاء بیولئژیکی داشته و در برگیرنده ایجاد و شکست پیوندهای کووالانس بوده که انرژی آنها بستگی به میزان اتمهای درگیر می باشد.
تا همین اواخر اثر ایزوتوپی فقط برای عناصر سبکی همانند H و C بررسی شده بود ولی استثناء ایزوتوپ حتی برای دورانهای کوتاهی در سالهای اخیر نیز گزارش شده است.
در حال حاضر تکنیک های ماس اسپکتروکوپیک (Mass Spectrocopic) دقیق اجازه اندازه گیری را که تا کنون غیر ممکن بوده است، میسر می سازد.

عاملهای تاثیر گذار در جابجائی و زیست دستیابی رادیونیوکلیدها در خاک:
1- جذب سطحی و واپاشی: (adsorption – desorption)
حرکت و جابجائی نیوکلیدها همانند سایر فلزات در خاک توسط جذب سطحی آنها روی ترکیبات ارگانیک و معدنی خاک محدود است.
در یک تقریب مناسب فلزات جذب سطحی شده در اولین حالت ممکن بی تحرک گشته و از حرکت و جابجائی آنها جلوگیری می گردد.
بدین ترتیب نقل و انتقال این گونه مواد رادیواکتیو و حداقل بخشی از آنها که درحالت محلول قرار دارند امکان واپاشی آنها میسر است، این وضعیت اساساً تمایل به تغییر پذیری نام دارد.
شواهدی وجود دارد که کاتیون های جذب سطحی شده بعضی از جابجائی های خود را حفظ کرده و هنگامیکه در ذرات خاک قرار می گیرند از طریق پیوند های کووالانس تا حدودی در خاک جابجا می شوند.
این مواد در گل و لای فشرده طبیعی یا دستکاری شده از حرکت و جابجائی بیشتری برخوردارند. ولی تعیین اثر آنها در خاکها، قدری مشکل است.
شواهدی که نشان دهد آنیونها بعد از جذب سطحی در سطوح خاک جابجا می شوند وجود ندارد .
جذب سطحی غالباً با استفاده از ضریب توزیع Kb کمی quantity(مقداری)می شود.نسبت غلظت ها در فازهای محلول و جذب شده ضریب توزیعKbنام دارد.
بدین طریق نسبت غلظت ها در فازهای معمول و جذب سطحی شده ،قابل تعین است. لازم به ذکر است که جذب سطحی واکنشی قابل برگشت بوده و ایجاد تعادل می نماید.
جذب سطحی معمولاً بصورت همزمان و کاملی، قابل برگشت نیست و فقط در مواردی محدود اتفاق می افتد. این فرایند مخصوصاً هنگامیکه در لایه های داخلی خاک وجود دارد،میسور است.
کاتیونها در لایه دوگانه قابل نفوذ خاک باقی می مانند. این وضعیت یک محدودیت مهمی برای مفهوم Kb ایجاد میکند، که غالباً به آن توجه نمی شود.
هیچگونه آماری در خصوص اینکه به چه دلیل جذب سطحی غیر قابل برگشت است، وجود ندارد هنگامیکه کاتیونها و آنیونها بسادگی از یک سطح واپاشی نمی شوند، اصطلاحاً بدون تحرک و ثابت قلمداد می مانند.
مخصوصاً در خصوص سزیم به نظر می رسد که تثبیت با توجه به مرور زمان افزایش یابد.
اخیراً مکنلی و دیگران با استفاده ازمیکروسکوپ و آنالیز با میکروکروب X-ray که نفوذ و انتشار جذب سطحی سزیم در لایه های درونی خاک بر روی میکا، شواهدی که جابجائی سزیم در لایه درونی خاک را نشان می داد،بدست آوردند.
سایر مکانیزم های تثبیت عبارتند از:
1- عناصر رادیواکتیو در سیستم های بیولوژیک وارد شده ونهایتا همراه مواد ارگانیک خاک ترسیب میشوند.
2- مواد رادیو اکتیو بصورت همزمان با مواد محلول خاک ترسیب میگردند.
به هر ترتیب جذب سطحی به شرایط آزمایشکاهی از قبیل زمان واکنش، استحکام یونی ، PH و ترکیب محلول که شامل مقدار مواد ارگانیک حل شده می باشد بستگی دارد.
جذب سطحی نیز ممکن است با توجه به نسبت محلول – خاک و یا شستشوی مکرر خاک، تحت تاثیر قرار گیرد.
بعلاوه کاهش زیست دستیابی ممکن است بدلیل تثبیت روی مواد معدنی خاک تغییریابد.
اما این مسئله ممکن است بدلیل تغییر توزیع فضای رادیو ایزوتوپها در خاک بعد از حرکت عمودی مواد بسمت پائین پروفیل خاک و نفوذ کند در تجمعات خاکی باشد.
برای آنالوگ های پایدار ،جذب سطحی رادیو نیوکلیدها بستگی به شرایط آزمایشگاهی نیزدارد.
هر گونه تغییر در شیمی عناصر و نه از طبیعت رادیواکتیو آن امکان بروز دارد.
بعنوان مثال:
جذب سطحی فلز قلیائی سزیم تا حدود زیادی بواسطه PH است.
در صورتیکه وابستگی PH برای اکسید آنیون ها نیز مورد انتظار است. همانند سلینت و سلنات برای انتقال موادی همچون نیکل، نقره ، رادیم و پالادیوم مورد انتظار است.
جذب سطحی فلزات در خاک غالباً بواسطه غلظت است.
مطالعات زیادی در خصوص سرنوشت فلزات در خاک ،جذب سطحی ایزوتوپها را ارائه می دهد.
از آنجائیکه محدوده مناسب غلظت برای رادیو نئوکلیدها طیف وسیعی را کمتر از عناصر پایدار شامل می شود.
لذا باید مواظبت جدی در خصوص قیاس اطلاعات و روندها به رادیو نئوکلیدها مورد توجه قرار گیرد.
برای نمونه خاک آلوده به فلزات سنگین می تواند چندین درصد وزن فلز را شامل شود. در صورتیکه خاکها در کشورهای بلاروس و اکراین که به طرز وحشتناکی آلوده137Csبودند که به دنبال حادثه چرنوبیل بیش از 555 KBqm-2 آلودگی ایجاد شده بود.
(1987 AEN; ساوه چنکو، 1995) این مقدار معادل در حدود9-10 مول بر کیلوگرم بود.mol kg-1
هنگامیکه یک رادیو نیوکلید به یک خاک اضافه گردد، آن خاک ممکن است قبلاً مقدار زیادتری ایزوتوپ پایدار داشته باشد.
لذا بیشتر واکنشهای سریع ،ترقیق ایزوتوپی خواهند داشت.
جذب و دفع رادیونیوکلیدهای فلزی توسط سیستمهای بیولوژیک خاک:
جذب و دفع رادیونئوکلیدهای فلزی توسط سیستمهای بیولوژیک خاک بستگی به ویژه گیهای شیمیائی و بیولوژیکی عنصر مورد نظر دارد.
میزان مراحل محدود کننده برای اکثر نئوکلیدها مخصوصاً آنهائیکه به واسطه ترکیبات خاک بی تحرک هستند در واقع حرکت و جابجائی آنها در فاز میانی بین محلول خاک و غشاء بیولوژیکی است.
اگر جذب سطحی سریعتر از حرکت ماده حل شده در فاز میانی باشد در چنین حالتی انتشار و پراکندگی آن محدود می گردد.
بنابراین ویژه گیهای جذب سطحی خاک تعیین کننده هستند.
از آنجائیکه وجود اکثر نیوکلیدها در خاک با فعالیت های انسانی مرتبط است، در چنین حالتی آنها بصورت همگن توزیع نمی شوند و رادیونیوکلیدهائی که توسط نزولات اتمسفری در محیط زیست پراکنده می شوند، در سطح خاک دپو گشته و غالباً بعد از دپوزاسیون (رسوب) برای سالهای متمادی در لایه های عمقی خاک نفوذ نمی یابند.
بنابراین گیاهان با ریشه های عمیق در معرض غلظت های بیش از حد این مواد (رادیونیوکلیدها) قرار نمی گیرند.
بدین ترتیب گیاهان ریشه دار در برابر آلودگی محافظت می شوند، برعکس اگر منبع آلودگی در زیر زمین قرار داشته باشد مثل آلودگی آبهای زیر زمینی از نشت تجهیزات انباری که در زیرزمین قرار دارند، آلودگی میسر می گردد.
پتانسیل ریسک انبار کردن عمیق ضایعات با میزان آلودگی بسیار بالا، در اولین مرحله گیاهان ریشه دار را آلوده می گرداند.
احتمال توزیع مجدد رادیو نیوکلیدها در لایه های عمیق خاک امکان آلودگی طیف وسیعی از گیاهان ریشه دار را فراهم می آورد.
هنگامیکه یک محلول رادیو اکتیو با فشار بیولوژیکی برخورد می کند، ممکن است اولین واکنش آن جذب سطحی باشد.
هنگامیکه عناصر طبیعی موجود باشد قبل از رسیدن رادیو ایزوتوپ تعادل ایزوتوپی برای حذف رادیو ایزوتوپ از محلول وجود دارد.
البته تشخیص آزمایشگاهی بین جذب سطحی و جذب معمولی قدری مشکل است.
تا کنون مطالعات زیادی در این خصوص انجام نشده است.
جذب سطحی صرفاً یک واکنش فیزیکی است، که در سطح اتفاق می افتد. ، در صورتیکه جذب نرمال یک فرآیند بیولوژیکی است و بواسطه نقش بیولوژیکی عنصر و ظرفیت موجودات زنده برای دستیابی به تهیه مواد مغذی ضروری و به منظور مقابله با عناصر سمی پتانسیل، تعیین می گردد.
وسعت و دامنه ئی که موجودات زنده در برابر رادیوایزوتوپها اتخاذ می کنند بستگی به نقش بیولوژیکی انها و شباهت هایشان به عناصر دیگر دارد.
بعنوان مثال:
سزیم (Cs)، نقش بیولوژیکی شناخته شده ئی ندارد و در عوض شباهت شیمیائی آن به پتاسیم(K) بدین معنی است که بواسطه مکانیزم های یکسان جذب می گردد.
به نظر می رسد تمایز K-Cs در گیاهان به غلظت نسبی و مطلق هر دو عنصر و حالت پتاسیم گیاهان بستگی داشته باشد.
تکنتیوم که همه ایزوتوپهای آن رادیواکتیو است، هیچگونه نقش بیولوژیکی ارزنده ئی ندارد و بنابراین اگر در غلظت های زیادی به اندازه کافی وجود داشته باشد که بتواند چرخه نیتروژن را مختل کند. در چنین حالتی است که سمی می شود.
سایر رادیو ایزوتوپها که می توانند بعنوان آلاینده های خاک وجود داشته باشند نیز سمی هستند.
این رادیو ایزوتوپها عبارتند از: کادمیم (Cs)، سرب (Pb) و سلینیوم (Se).
واقعیت این است که تخریب رادیو ایزوتوپها به منظور تولید اشعه های یونیزه،نقش بیولوژیک آنها را تحت تاثیر قرار نمی دهد.
رادیو ایزوتوپهائی که جذب می شوند همانند ایزوتوپهای پایدارشان نیز دفع می گردند.
ممکن است آنزیمها بین ایزوتوپهای یک عنصر به اندازه کافی حساس بوده و تا حدودی متمایز گردند که این مهم منجر به تغییرات در فراوانی نسبی ایزوتوپی میگردد، ولی در هر صورت اثر آن کم است. (مرچال و دیگران 1999)
توزیع مجدد رادیوایزوتوپها در یک گیاه یا سایر سیستم های زنده تا حدود بسیار زیادی همانند ایزوتوپهای پایدار آنها خواهد بود.
در زمانیکه سطوح رادیواکتیویته خیلی بالا باشد ممکن است تخریب ژنتیکی ایجاد گردد، ولی در سطوج پائین تر نیز مواد غذائی برای مصرف، نامناسب تلقی می گردند.
بدین ترتیب از آنجائیکه گیاهان و سایر موجودات زنده از اثرات جانبی ناشی از تجمع رادیو ایزوتوپ ها در بدنشان آزار نمی بینند.
لذا، آنها برای توسعه استراتژی برای مقابله با خطرات رادیواکتیو محدود کردن تجمع رادیوداروها در بدنشان، تحت فشار قرار نمی گیرند.
البته تعدادی استراتژی از قبیل، کمپلکسیون (complexation) (واکنش شیمیائی بین یون فلزی و هویت مولکولی (لیگاند) که حداقل یک اتم یا یک جفت الکترون به اشتراک گذاشته نشده تشکیل یک مجموعه پیچیده را می دهند) و پریسیپیتاسیون (precipitation)، برای مقابله با غلظت های افزایش یافته عناصر که بصورت پتانسیل سمی هستند توسط موجودات زنده توسعه می یابند و بدین طریق تجمع عناصر در بدن موجودات کاهش می یابد و حتی ممکن است در مواری سبب تجمع بیش از حد گونه های رسوب یافته و کمپلکس ها گردد.
البته این استراتژیها بندرت برای کاهش خسارتهای مواد رادیواکتیو و یا مهم تر اینکه، کاهش آلودگی زنجیره غذائی، مفید تلقی می شوند.
بعبارت دیگر، استراتژیهای بیان شده فوق، برای کاهش مواد رادیواکتیو و کم کردن آلودگی زنجیره غذائی مفید نمی باشند.
هنگامیکه عناصر رادیواکتیو تحت عنوان یک آلاینده شیمیائی مطالعه شوند، و یا در مبحث مربوط به رادیو اکولوژی ( مواد رادیو اکتیو محیط زیست) قرار گیرند، باید مواظبت و مراقبت جدی در خصوص انتقال داده ها، مدنظر قرار گیرد.
این دقت بخاطر آن است که بعضاً مشاهده می شود که غلظت های یک آلاینده شیمیائی خیلی متفاوت است و ثانیاً سیستمهای بیولوژیک خودشان را با مواد رادیو اکتیو، تطابق داده و در حضور یک آلاینده شیمیائی حتی فراتر از آستانه تحمل شان، واکنش نشان می دهند.
این چنین تغییراتی در حضور ماده رادیو اکتیو که مقدار آن ناچیز است، امکان ظهور و بروز ندارد.
برای مثال:
ممکن است Se در غلظت های بالا (زیاد) وجود داشته باشد، در چنین حالتی میکروارگانیزمهائی شناسائی شده اند که قادرند Se اولیه را به منظور حذف مسمومیت آن، در همان ابتدا ترسیب نمایند.(Roux etal 2001).
گوتری و تورنی (Coughtrey و Thorne) در سال 1983 میلادی مطالعات فوق را انجام داده اند.
البته آژانس بین المللی انرژی اتمی و اتحادیه بین المللی رادیو اکولوژیکی بترتیب در سالهای 1994 و 1989 بانک های اطلاعاتی را جمع آوری کرده اند.
معمولاً اطلاعات برای گیاهانی که بسهولت می شود از آنها نمونه گیری کرد و عمدتاً از قسمت های روی زمین و نه ریشه ها جمع آوری شده است، البته در مواقعی نیز قسمت های خوراکی گیاهان(edible) نیز بصورت انتخابی مورد مطالعه قرار گرفته و اطلاعات آنها به ثبت رسیده است.
خلاصه اینکه اطلاعات محدودی در خصوص سایر (موجودات) سیستم های زنده که در خاک حضور دارند، وجود دارد.
نقش میکروارگانیسم های (microorganisms) موجود در خاک در تعیین سرنوشت رادیو نیوکلیدها در سال 1999 به واسطه آقای گاد Gadd، مرور شده است.
از طرف دیگر به نظر نمی رسد (unlikely) میکروارگانیزمهای خاک سینک(sink) مناسبی برای رادیونیوکلیدهای که بصورت بسیار قوی جذب سطحی شده اند، باشند.
این موضوع به خاطر آن است که جذب سطحی رادیونیوکلیدها در ترکیبات خاک اثر آنها را مستقرق می کند.
در هر صورت علی رغم مشکلات آزمایشگاهی که اندازه گیره ها را مختل (hamper) می نماید، این امکان وجود دارد که نگرش صرفاً غیر هوازی برای بی تحرک کردن رادیونیوکلیدها در خاک فرآیندهائی را که ممکن است برای رادیونیوکلیدهای که جذب سطحی کمتری دارند و عناصری که بسهولت زیست دست یاب هستند، مورد چشم پوشی قرار دهد.
عناصری همانند Tc, Se در موارد فوق صادق است.
سیستمهای بیولوژیکی براحتی بعنوان یک سینک منفعل در رابطه با فلزات عمل نمی کنند.
بلکه این سیستمها نیز محیط شیمیائی خود را تغییر داده و در تعاقب آن گونه های شیمیائی نیز تغییر می کنند.
نهایتاً جابجائی مواد غذائی و عناصر پتانسیل سمی نیز دچار تغییر می شوند. البته تاثیر سیستمهای بیولوژیکی بر رادیونیوکلیدها، نسبت به سایر فلزات از مطالعات کمتری برخوردار بوده است.
ولی قطعاً گسترش مطالعات در خصوص تاثیر سیستمهائی بیولوژیک مواد رادیواکتیو امری ضروری و اجتناب ناپذیر است.
عاملهای مربوط و مناسب برای مطالعه در خصوص تاثیر رادیونیوکلیدها، عبارتند از: PH، پتانسل های اکسیداسیون و احیاء (Redox)، غلظت لیگاندهای کمپلکس دار متحول و فرسایش مواد معدنی(mineral weathering) موجود در خاک را میتدان نام برد.
البته اهمیت نسبی، بستگی به خاک و شیمی عنصر مورد بررسی(مطالعه) دارد .
جای تعجب نیست که عناصری همانند سلینوم(Selenium)(Se) و تکنتیوم (Teehnetium) (Tc) که در حالت های مختلف اکسیداسیون هستند به شرایط اکسیداسیون و احیاء (Redox) حساس باشند.
برای سایر عناصر، احتمال اثر غیر مستقیم نیز وجود دارد.
برای مثال:
احتمال دارد آمونیومی (amononium) که تحت شرایط احیاء بوجود آمده است، جذب سطحی Cs را متوقف نماید.
سایر اثرات غیر مستقیم احتمالی وابسته به اکسیداسیون و احیاء از هم پاشیدگی ترکیبات خاکی است که در ویژه گیهای جذب سطحی خاک مشارکت دارند.
هیچ وابستگی ph از جذب سطحی سزیم در مواد معدنی خاک بجز تحت شرایط حاد هنگامیکه فرسایش سریع صورت پذیرد، وجود ندارد.
در صورتیکه جذب سطحی اغلب فلزات گذار (Transit) ، Ni، Ag، pd و زیرکونیم و همچنین اکسی آنیونهائی (oxyanions) مانند -TcO3، -2SeO4 و-2SeO3، در طیف وسیعی از PH متفاوت هستند.
جذب سطحی سزیم(Cs) در بعضی از مواد معدنی گل و لای (خاک رس) کاملاً گزینشی (Selective) بوده و این مهم به نحو قابل ملاحظه ای در خصوص مواد معدنی خاک رس صادق است.
این گزینش بنحو گسترده ئی به فرسایش و وجود پوشش های معدنی – آلی بستگی دارد.(mues et al 1999).
چنین اثراتی برای سایر رادیونیوکلیدهای رایج (common) در خاک گزارش نشده است.
نهایتاً اینکه حلالیت فلزات گذار (Transit) به واسطه فرماسیون(تشکیل) لیگاندهای کمپلکس (Complex) ،
در محلول افزایش می یابد.
اما هیچ مکانیزم اکویوالانی (مشابهی) برای فلزات قلیائی (alkali) مثل Rb و Cs ویا شبه آنیونها همانند Sc و Tc وجود ندارد.
استراتژیهای ری مدیاسیون (اصلاح و درمان):
بهترین استراتژی برای حذف آلاینده از خاک(همانند تمام آلودگی ها) به صورت ذیل قابل تصوراست:
هنگامیکه یک خاک آلوده می گردد، روشهای مختلفی برای کاهش اثرات وجود دارد.
این روشها تا حدود زیادی مشابه روشهائی است که برای کاهش الاینده های فلزی مورد استفاده قرار می گیرند.
روشها عبارتند از:
1- تثبیت گیاهی . (phytostabilization)
2- عصاره گیری گیاهی . (phytoextraction)
3- انتخاب محصولات و گیاهی غیر خوراکی . (nonfoodcrops)
4- تصحیح خاک به منظور کاهش و یا افزایش جذب.
5- انجام عملیات کشاورزی نیمه صنعتی مثل، پوشاندن و رقیق کردن خاکهای آلوده با خاکهای پاک. (clean soil).
تمامی روشهای فوق در مقاله مربوط به کنترل آلودگی در همین سایت بتفصیل آمده است. (رجوع به مقاله کنترل آلودگی خاک در همین سایت).
در هر صورت و صد البته نباید فراموش کنیم که تفاوتهای عمده و مهمی بین رادیونیوکلیدها و سایر آلاینده های فلزی وجود دارد.
این تفاوتها بترتیب و درجه اهمیت عبارتند از:
1- بعید است که این آلاینده ها اثرات نامطلوبی بر تولید محصول یا فعالیت بیولوژیکی داشته باشند،البته مناطق آلوده شده استثناء است.
2- اثر استفاده از سرزمینی که در معرض رادیواکتیو قرار می گیرد باید مورد بررسی قرار گیرد.
عاملهای مختلفی که در این خصوص مدنظر قرار خواهد گرفت عبارتند از:
آلودگی آبهای سطحی توسط فرسایش و روان آب، جابجائی و بلعش گرد و خاک، مصرف خاک توسط حیوانات و انسانها بواسطه سبزی های خوب شسته نشده، استنشاق و فرو بردن گرد و خاک در گلو و مصرف مستقیم خاک توسط بچه ها و نابالغین و در معرض قرار گرفتن کارگران کشاورزی و سایر استفاده کننده گان از سزمین، هنگامیکه خاک توسط تشعشعات(تابش ها) گاما آلوده می گردد.
3- تعیین ریسک دوز (مقدار) تجمعی برای یک جمعیت و نه فقط افراد ،باید مورد توجه قرار گیرد.
این مهم بدین خاطر است که ریسک سرطان ها برای یک جمعیت متناسب با کل کسانی است که در معرض آلودگی قرار می گیرند.
این نگرش بصورت کمتر سیستماتیک برای سایر اشکال آلودگی نیزکاربرد دارد.
منابع و سرنوشت تعدادی از رادیونئوکلیدها در خاک به قرار ذیل است:
جدول فوق، ایزوتوپهای فلزی و نیز شبه فلزات ، که از نظر محیط زیستی مهم هستند نشان رامی دهد.
شکل ذیل نیز تعدادی از گدازه های نیوکلیدهای رادیواکتیو را در محیط زیست به تصویر می کشد.
1- عنصر کبالت. (Cobalt):
این عنصر دارای عدد اتمی 27 است و فقط یک ایزوتوپ پایدار طبیعی دارد.
Co 59دارای فراوانی 100درصدی است ودارای تعداد 22 رادیو نیوکلید است که شامل Co 56 57Co, 58Co, 60Co میشود از این رادیو نیوکلیدهای فوق فقطCo 60 دارای نیمه عمر فیزیکی 5.27 سال بوده واز اهمیت محیط زیستی قابل ملاحظه ئی برخوردار است.
بدین ترتیب کبالت -60 توسط فعال شدن نوترون کبالت پایدار، تولید گشته و بواسطه تابش های بتا تجزیه و متلاشی می گردد.
البته تابش های بتا توسط تابش دو اشعه گاما با انرژی نسبتاً بالا در 1173 و 1332 kev همراه است.
نهایتاً اینکه کبالت 60 به نیکل غیر رادیواکتیو تجزیه و متلاشی می شود(60Ni ) 60Co بخاطر تابش اشعه گاما مناسب کاربردهای صنعتی فراوانی است.
این کاربردها عبارتند از:
پرتونگاریهای مقطعی مثل سی تی اسکن مغز، رادیو تیراپی (پرتودرمانی) و استرلیزاسیون مواد غذائی و ابزارآلات پزشکی. کبالت همچنین بعنوان یک آلاینده در استیل های تابش داده شده در تجهیزات هسته ئی تولید می گردد.
کبالت- 60 ناشی از ضایعات مختلف هسته ئی وارد محیط زیست می گردد.
حرکت این ماده آبزی و خاکزی توسط بوفتری و تونی در سال 1983 مورد مطالعه قرار گرفته است.
کبالت پایدار در انواع خاکها از فراوانی نسبی برخوردار است و غلظت های آن دامنه ئی از 0.05 تا 65 میلی گرم در کیلوگرم است.
بوون (Boven)در سال 1979 بیان کرد که غلظت متوسط کبالت پایدار در خاک 8 میلی گرم در کیلوگرم است.
ولی اسمیت در سال 1994 بر اساس تحقیقاتی بیان نمود که دامنه غلظت های کبالت پایدار در خاکها 0.05 تا 300 میلی گرم در کیلوگرم است. دامنه میانگین 10 تا 15 میلی گرم در کیلوگرم کبالت برای گیاهان یک عنصر ضروری محسوب می شود.
البته این دامنه برای کلیه گیاهان از قارچها و جلبکهای سبز و ابی تا گیاهان تنومند است.
ولی به این نکته باید توجه داشت که کبالت نقش بسیار مهمتری در میکروارگانسیم ها بازی می کند.
غلظت های کبالت پایدار در گیاهان آوندی (مجرا دار) محدوده ئی از 0.005 میلی گرم در آنجیو اسپرمهای چوبی تا 4.6 میلی گرم در کیلوگرم در سبزیجات علفی است.
لازم به ذکر است که چندین گونه گیاه برای تجمع کبالت بعنوان شاخص و تجمیع پذیر کبالت شناسائی شده اند. (روکس و دیگران در سال 1977)
کبالت همچنین در حالت های +2 یا +3 ظرفیتی (والانسی) وجود دارد و با مواد ارگانیک براحتی کمپلکسیون هائی، شکل می دهد.(ایجاد مواد مرکب)
اسید استیک و EDTA (اتلین دی امین تترا استیک اسید) بصورت معمول برای استخراج کوبالت از خاکها مورد استفاده قرار می گیرند،این عمل تقریباً منجر به 70% استخراج کبالت می گردد.
این نکته باید اضافه شود که پتانسیل ذهکشی خاک و مجموعه واکنش های اکسیداسیون احیاء نقش فوق العاده بارزی در کنترل زیست دستیابی کبالت در خاکها ایفا می نمایند.
خاکهای مرطوب از پتانسیل اکسیداسیون احیاء کمتری برخوردار بوده و اسید استیک بیشتری برای استخراج کبالت نیاز دارند.
در صورتیکه خاکهای خشک از پتانسیل اکسیداسیون بیشتری برخوردارند. (میت چل و دیگران در سال 1957)
ممکن است این اثر بخاطر تمایل کبالت به جذب اکسیدهای منگنز در خاک باشد.
قابلیت انحلالی که بصورت بسیار قوی توسط پتانسیل اکسیداسیون احیاء تحت تاثیر قرار می گیرد و ممکن است کوبالت با افزایش زمان ماند، در خاکها جایگزین کریستالهای منگنز گردد.
در هر صورت رها سازی کبالت 60 در خاک برای محصولات کشاورزی بیش از حد مجاز خطرات فراوانی را در بر داشته و می تواند از طریق زنجیره غذائی وارد سیستمهای زنده گردد.
بدین ترتیب لازم است برای در امان نگه داشتن خاکهای حاصلخیز کشاورزی از ورود بیش از حد این ماده به خاکها جلوگیری گردد.
2- سلنیوم : (Selenium) با عدد اتمی 34
سلنیوم اگر چه به معنای واقعی یک شبه فلز نیست ولی بعضی از ویژه گیهای فلزی را برخوردار دارد.
این موضوع بخاطر اهمیت محیط زیستی بعضی از رادیوایزوتوپهای آن می باشد.
این شبه فلز دارای 26 ایزوتوپ است که 6 تای آن پایدار بوده و در محیط زیست بصورت طبیعی وجود دارند.
دوتا از ایزوتوپهای آن از اقبال محیط زیستی بیشتری برخوردار بوده و عبارتند از:
Se70 با نیمه عمر 106 ×1.1 و سلنیوم 75 (Se75) که دارای نیمه عمر 119 روز است که غالباً بعنوان ردیاب از آن استفاده می شود.
ارزیابی های تعیین ریسک مختلفی برای شناسائی سلنیوم 79 (79Se) نیز مورد توجه قرار گرفته است این احتمال وجود دارد که این عنصر در هنگامه امحاء ضایعات، وارد زیست کره گردد.
مطالعات گسترده ئی در خصوص سلنیوم پایدار صورت گرفته است و این موضوع بخاطر آن است که این عنصر یک ماده غذائی ضروری برای حیوانات و باکتری ها محسوب می شود.
البته این عنصر در بعضی از محیط های طبیعی بصورت پتانسیل سمی بوده و در اکوسیستم های آلوده به این عنصر نیز مطالعه شده است.
میزان سلنیوم در انواع خاکها در حدود 0.4 میلی گرم در کیلوگرم است.
خاک هائیکه زیر 0.2 میلی گرم در کیلوگرم سلنیوم دارند، بعنوان خاک های با سلنیوم ناکافی شناخته شده اند و خاک هائی که بیشتر از 5 میلی گرم در کیلوگرم سلینوم دارند بعنوان خاک سلنیوم دار قلمداد می گردند.
سلنیوم غالباً در حالت2- یافت می شود و سلنید ها معمولاً همراه با سولفیدها در معادن سنگ فلزی وجود دارند.
سلنیوم عنصری و همچنین دو نوع اکسی آنزیمهای آن شامل سلنیت و سلنات (SeO32- , SeO42-) نیز ممکن است در خاکها و فراماسیون های جیولوژیکی وجود داشته باشد.
اکثر تحقیقات مربوط به سلنیوم نگرانی های را در خصوص سیستم های آلوده شده و سیستم های که بصورت طبیعی غنی هستند ، با خود همراه دارند.
این نگرانی ها مربوط به مسمومیت سیستم های بیولوژیک و اینکه چگونه گونه های زنده غلظت های بالای سلنیوم را تحمل می کند را نیزدر بر می گیرد.
البته عکس این قضیه نیز صادق است و آن اینکه کمبود سلنیوم و ارتباط بین محتوای سلنیوم گونه ها و هجمه و شدت علائم نیز مد نظر است.(تان و دیگران در سال 2002)
البته هنگامی است که وجود رادیو سلنیوم منجر به نگرانی میگردد، تمامی مطالعات فوق ضرورتاً نمی توانند به همه موفقیت های بیان شده تعمیم داده شوند.
اگر سطح سلنیوم پایدار پائین باشد در این خصوص مجموعه بازنگری ها بشرح ذیل است:
1- گونه ئی شدن عنصر سلنیوم بطرز مستحکمی بستگی به شرایط اکسیداسیون و احیاء دارد. (جایاویرا و بیگار 1996 ) (Jayaweera & Biggar 1996)
2- فعالیت میکروبی نیز مهم است. (نیل Neal در سال 1995)
3- سلنیت و سلنیوم عنصری تحت شرایط هوازی به آرامی به سلنات و سلنیت اکسیده می شوند.
4- نمکهای هر دو یعنی سلنات و سلنیت بجز در خاکهای بشدت اسیدی، کاملاً قابل حل بوده و از حلالیت بالائی برخوردارند.
جائیکه MnSeO3- ممکن است بصورت جزئی قابل حل باشد.(الرشیدی و دیگران Elvashidi etal 1987)
گونه های اصلی سلنیوم در شرایط محلول با اکسیداسیون و احیاء بالا PH + Pe > 15 که SeO42- است.
در صورتیکه SeO32- و HSeO3- در شرایط واسط (PH + Pe 7.5 + 15) ، با HSe- در اوزان اکسیداسیون احیاء پائین تر و H2Se وجود فقط در PH خیلی پائین غالب هستند.
دلالت هائی وجود دارد که حالت اکسیداسیون سلنیوم ممکن است تحت تاثیر تغییرات محلی در شرایط اکسیداسیون و احیاء در ریزوسفرها قرار گیرد. (وو و دیگران در سال 1997) Wu , etal
لازم به ذکر است که سلنات در خاک تا حدود زیادی همانند سولفات عمل می کند، و به این دلیل جذب سطحی مستحکمی ندارد. (اسپوزیتو در سال 1989) Sposito
سلنیت با کاهش جذب سطحی در قبال افزایش PH و در حضور آنیون های رقابت کننده ای مانند فسفات بنحو شایسته ئی جذب سطحی می گردد.
از دو اکسی آنیون فوق (Oxyanions) سلنات تحرک کمتری دارد. و این موضوع بدلیل آن است که از جذب سطحی مستحکم تری برخوردار است.
بنظر می رسد که سلنات بصورت مستقیم سمی نباشد ، بخاطر این که این ماده در اولین مرحله به سلنیت تبدیل می شود. (تورنر و دیگران در سال 1998) Turner etal
متیالاسیون زیستی (biomethylation) یک خصوصیت ضروری برای دینامیک (dynamic) سلنیوم در خاک است.
این مکانیزم (متیالاسیون زیستی (biomethylation) توسط میکروارگانیزم های ارگانیک و سلنیوم معدنی تحت شرایط هوازی و غیر هوازی بوجود می آید . (الکساندر و دوران در سال 1977) Doran & Alexander
به نظر می رسد که قارچها موجودات غالبی هستند که مکانیزم متیلاسیون (methylation) را در شرایط هوازی بر عهده دارند و بر عکس باکتری ها هنگامیکه شرایط غیر هوازی است (anaerobic) موجودات غالب methylationهستند.
این عمل باکتری ها ،بخاطر آن است که آنها بصورت ساختگی در جدا سازی دخیل هستند.
تصحیح و درمان خاک قلیائی با سلنیوم از طریق فراریت آن با توجه به غنی سازی که صورت گرفته است بنحو گسترده ئی مطالعه شده است.
این تحقیق عمدتاً در رابطه با کربوهیدراتها صورت گرفته است.(Carbohydrates)
در هر صورت اشکال فرار عمدتاً دی میتل سلنید (dimethyl selenide) و دی میتل دی سلنید (dimethyl di selenide) ممکن است با ترکیبات خاک وارد واکنش شوند. (زیوو و پیترسون 1985) Zieve & Peterson
این واکنش مخصوصاً با مواد ارگانیک و میکروارگانیزم های خاک میسر می گردد. (دونگان و دیگران 2002) Dungan etal 2002
بدین ترتیب سلنیوم توسط نقل و انتقالات بیشتری مجدداً جابجا می گردد.
میتل سلنیوم (methyl – Se) تحت شرایط غیر هوازی توسط میکروارگانیزم های متانوژون (methanogen) و باکتری های کاهنده سولفات (sulfate – reducing bacteria) تجزیه گشته و خورد می شود.
شرایط سیلابی(جاری سازی) نیز شار مولکولهای فرار را کاهش داده و باعث افزایش زمان ماند آنها در خاک می گردد.
بدین ترتیب این احتمال وجود دارد که مولکولهای فرار قبل از اینکه در خاک رهاسازی شوند، به لحاظ شیمیائی و میکروبی ،
غیر متحرک گردند.
(زانگ و فرانکن برگر 1999-2000 و 2002) Zhang & Franken berger
میکروارگانیزم های خاک نیز ممکن است سلنیوم اولیه را به سلنید و سلنات اکسیده کنند.
در هر صورت کاهش سلنیت و سلنات به سلنیوم اصلی توسط میکروبها مهمتر بوده و مطمئناً مستلزم تحقیقاتی بیشتر از اکسیداسیون میکروبی است.
باکتری ها و قارچ ها نقش مهمی در کاهش سلنیوم بازی می کنند ،البته باکتری ها بنحو گسترده تری مورد مطالعه قرار گرفته اند.
بخاطر اینکه باکتریها سلیننیوم را تحت شرایط غیر هوازی کاهش می دهند .( بلوم و دیگران 1998) Blum . etal
امکان دارد سلنیت و سلنات توسط باکتری ها تحت شرایط هوازی با استفاده از ترمینال پذیرنده های الکترونی
(Terminal electron acceptors) برای تنفس توسط باکتری ها مورد استفاده قرار گیرند.
مضافاً اینکه نشان داده شده است باکتری هائیکه که سولفات تنفس می کنند نیز می توانند تا حدودی مورد استفاده قرار گیرند.
این باکتری ها از سیستم های آنزیمی دیگری (enzymatic) برای تنفس سلنیوم استفاده می کنند.
دخالت های تنفسی (No3) نیز کراراً گزارش شده است. آنزیمهای کاهنده (reductases) نیز فقط برای چند باکتری مشخص شده است.
این باکتری ها عبارتند از:
1- تایورا سلناتیس (Thauera selenatis)
2- انتروباکتر کولاسی (Enterobacter cloacae)
3- سولفورس پیری لیوم برانسیل(sulfurospirillum branesil)
سلنیوم اصلی و اولیه می توانند به مقدار بسیار زیادی تجمع پیدا کرده، یا در محیط پخش و پراکنده گردند. (لوسی و فرانکن برگر 1997) Losi & Frankenberger
گیاهان همچنین با توجه به جذب سلنیوم و ظرفیت تجمع پذیری غلظت های سمی بصورت پتانسیل بالا ،متفاوت هستند.
گزارش شده است که گیاهان سرزمین های مرطوب(تالاب ها) سلنیوم را تبخیر می کنند و عاملهای تاثیر گذار بر تبخیر توسط آقایان تری و زاید (Terry & Zayed) در سال 1994 مرور گردیده است.
همانگونه که در بالا توضیح دادیم، پیشنهاد شده است که تغییرات در شرایط اکسیداسیون و احیاء در ریزوسفرهای
( ناحیه ئی از خاک که به صورت مستقیم تحت تاثیر ترشحات ریشه ی گیاهان و میکرو ارگانیزمهای خاک قرار دارد)بعضی از گیاهان ممکن است گونه ئی شدن سلنیوم را در خاک تحت تاثیر قرار دهد.
بعضی از گونه های گیاهی سلنیوم را در خاکهای غنی از سلنیوم تجمع می نمایند، ولی این تجمع پذیری به اندازه ئی که برای فلزات سمی مانند کادمیم و نیکل که از خاصیت تجمع کننده گی بالائی برخوردارند، نمی باشد. (سری واستاوا و دیگران در سال 2005)Srivastawa
اخیراً چندین مطالعه در خصوص جذب سلنیوم در خاکها با سطوح سلنیوم نرمال و کم صورت گرفته است.
موقعیت احتمالی در مورد آلودگی رادیو سلنیوم مشخص گردیده است، ولی اطلاعات و داده ها بنحو بسیار جامع تری توسط گافتری و دیگران در سال 1983(Coughtrey) مورد بررسی قرار گرفته است.
استورنتیوم (Strontium) : با عدد اتمی 38
استورنتیوم (Sr) یک فلز خاکی قلیائی است که دارای چهار ایزوتوپ طبیعی پایدار می باشد.
این چهار ایزوتوپ عبارتند از: Sr88،, 86Sr, 87Sr, 84Sr
ایزوتوپهای با عمر کوتاه در پزشکی و بعنوان ردیاب ها مورد استفاده قرار می گیرد.
این ایزوتوپها عبارتند از:Sr90 89Sr, 85Sr, 82Sr
ولی ایزوتوپ Sr 90 ازطولانی ترین عمر یعنی 29 سال برخوردار بوده وقادر است در محیط زیست پراکنده شده.
منابع پراکنش 90Srدر محیط زیست عبارتند از: آزمایشات جنگ افزارهای اتمسفری، تشعشعات ناشی از راکتورهای هسته ئی و یا کارخانه های بازفراوری و گرد و غبارهای اتمی ناشی از حادثه چرنوبیل را می توان نام برد.
استورنتیوم، آنالوگ شیمیائی (شبه) کلسیم است و نقش بیولوژیکی شناخته شده ئی ندارد.
سیستم های بیولوژیکی از تشخیص بسیار ضعیفی بین کلسیم و استورنتیوم (Sr) برخوردارند.
شیمی استورنتیوم در انواع خاکها بسیار ساده تر از سزیم (Cs) است.
در چنین حالتی نه تنها کوارگانیسم شیمی آن ساده است بلکه جذب سطحی آن نیز روی ترکیبات خاک ارگانیک و معدنی نیز تا حدود بسیار زیادی غیر انتخابی است.
فرآیندهای تثبیت و یا طول عمر قابل ملاحظه ئی از Srگزارش نشده است.
این موضوع بدین معنی است که استورنتیوم می تواند در سیستم های خاک بصورت مداوم بازیافت گردد.
بدین ترتیب خطر رادیواکولوژیکی آن نسبت به زمان کم نمی شود.
شباهت شیمیائی بین استورنیتوم و ماده غذائی ضروری همچمون کلسیم و نیز تمایز بیولوژیکی ضعیف بین آنها (دو عنصر) در واقع کلید تعیین اثر رادیولوژیکی این آلاینده است.
استورنتیوم همانند کلسیم می تواند توسط گیاهان بصورت مستقیم جذب گردد. این عمل می تواند از طریق برگها صورت گیرد. (کارینی و لومبی 1997)Carini & Lombi
در هر صورت مسیر اصلی برای ورود استورنتیوم به زنجیره غذائی از طریق جذب خاک – ریشه است.
کلسیم یک کاتیون اصلی در اکثر خاکها محسوب می گردد. و بعنوان کاتیون قابل تبادل جذب سطحی شده و برروی سطوح با بار منفی ترکیبات خاک و نیز همراه با جزئی از کربنات های قابل حل عمل می کند.
استورنتیوم در کربناتها و کمپلکس های مبدل که از مواد معدنی خاک رس، مواد آلی و اکسیدهای آهن، منگنز و آلومینیوم تشکیل شده است جایگزین کلسیم می شود.
جابجائی استورنتیوم در خاک تا حدود زیادی بستگی به ظرفیت تبادل کاتیونی دارد، بنابر این ، بافت، مواد معدنی شناسی و محتوای مواد ارگانیک نیز در جابجائی استورنتیوم موثر هستند.
کلسیم و استورنتیوم بر خلاف فلزات ترانزیت ،کمپلکسون های کواوردی نانس(هماهنگ) با لیگاندهای ارگانیک تشکیل نمی دهند.
بنابراین امر آنها مواد ارگانیک قابل حل بی اثری هستند.
بدین ترتیب آنها ممکن است فلزات ترانزیت را حل کنند، ولی هر دوی آنها جذب سطحی فاز جامد مواد ارگانیک می شوند.
این عمل بواسطه ظرفیت تبادل کاتیونی موثر می گردد، هنگامیکه محتوای مواد معدنی خاکها کم باشد، نقش مواد ارگانیک در بی تحرک سازی استورنتیوم در خاکهای کاملاً ارگانیک بسار مهم است.
این خاکها عبارتند از: خاکهای جنگل و خاکهائی ماسه ئی.
استورنتیوم نسبت به کلسیم توسط مواد ارگانیک از قابلیت ابقاء کمتری برخوردار است.
عکس این روند نیز برای تبادل این ماده روی مواد معدنی گل و لای نیز مشاهده شده است.
این حالت برای اغلب خاکها در اروپای شرقی که بنحو شدیدی توسط گرد و غبارهای اتمی ناشی از انفجار چرونوبیل آلوده شده اند مشهود است.
عامل انتقال خاک به گیاه با افزایش محتوای مواد ارگانیک کاهش می یابد.
هنگامیکه استورنتیوم با مواد ارگانیک همراه باشد بخش های سبکتر مواد ارگانیک از قبیل اسیدهای فولوئیک بسیار فعال به نظر میرسد.
PH خاک نیز اثر بسیار مهمی بر جابجائی استورنتیوم و جذب بیولوژیکی آن دارد.
اول اینکه جذب سطحی استورنتیوم روی ترکیبات خاک وابسته به PH خاک است و برای تعداد زیادی از خاکها جذب سطحی بیشتر در خاکهای کلسیمی با PH بالا است و ممکن است مقدار رسوب Srco3 روی خاک جئوتیت (goethite) غشاء های بیولوژیکی نیز به PH وابسته باشد.
از آنجائیکه ظرفیت تبادل کاتیونی ریشه ها و سایر غشاء ها بدلیل ضعیف بودن گروه های عملیاتی اسید ضعیف می باشد، لذا بدلیل این اثر، PH بر جسته می گردد.
(یرماکوف و مچیک 1999) Yermakov & meychik
واکنش های Sr با خاک تا حدود بسیار زیادی لحظه ئی و قابل برگشت هستند.
Instantaneous & reversible البته Couphtrey & Thorn 1983 سلسله ائی از استورنتیوم غیر قابل تبادل را در خاکهای مختلف بین 3 و 33 درصد ذکر کرده اند.
مکانیزم جذب سطحی استورنتیوم در اغلب سطوح خاکهای مختلف تا حدود بسیار زیادی جذب سطحی فیزیکی است.
البته تشکیل کمپلکسیون های ضعیف در لایه خارجی خاک محتمل است.(ساهائی و دیگران 2000) Sahai etal
جذب سطحی استورنتیوم در هر حالتی به سهولت قابل برگشت بوده و نفوذ قابل ملاحظه ی استورنتیوم به مکان های داخلی اکسیدهای خلل و فرج دار منتقل شده و منجر به تثبیت آن می گردد.
هیج نشانه مستحکمی در خصوص کاهش زیست دستیابی استورنتیوم با زمان بدلیل تثبیت کند جذب سطحی در حال انجام یا طولانی شدن زمان جذب، وجود ندارد.
البته نشانه هائی از جذب سطحی ویژه در اکسیدهای هیدراته یا آهن و آلومینیوم وجود دارد و تشکیل کمپلکسیون ها روی لایه داخلی هماتیت قابل مشاهده است.
کاهش آشکار جذب شدن استورنتیوم در طول مدت یک دوره چهارماهه در خاکهای در معرض سیل بدلیل تغییر شرایط خاک بدون دخالت تثبیت، توسط وانگ و استانتون در سال 2005 (Wang & Staunton) گزارش شده است.
زیرکونیوم (Zirconium) : با عدد اتمی 40
این رادیو نیوکلید دارای 5 ایزوتوپ پایدار با فراوانی طبیعی متفاوت است:
Zr(51.5%), 91Zr(11.2%), 92Zr(17.1%), 94Zr(17.4%), 96Zr(2.8%) 90
و 8 ایزوتوپ رادیو اکتیو دیگر شامل:
Zr, 88Zr, 89Zr, 93Zr, 95Zr, 97Zr 86می باشند.
از ایزوتوپهای رادیو اکتیو فوق فقط Zr95 به لحاظ آلوده کردن محیط زیست به طرز فوق العاده ئی با اهمیت است.
این فلز رادیواکتیو بواسطه واکنشهای شکافت (Fission) و نیز توسط فعال شدن نوترون Zr 94تولید می گردد.
نیمه عمر فیزیکی آن 64.2 روز است.
Zr 95در طول زمان بهNb 95 و Nb95m تجزیه می گردد.
95 Zr درنتیجه انفجارات ناگهانی جنگ افزارهای هسته ئی ، تخلیه پسماندهای رادیو اکتیو و نیز حادثه چرنوبیل (Chernobyl)، جائیکه آلودگی قابل ملاحظه ائی به علت پراکنش تابش میله های سوخت راکتور
در محیط زیست محلی بوجود آمده است.
بورووی ( Borovoi etal) و دیگران در سال 1988 تخمین زده اند که سوخت راکتور چرنوبیل به میزان 3.3 X 1010 Bqg-1 زیرکونیوم بوده است.
95Zr توسط تابش های بتا با انرژی ماکسیمم بتا (Emax) که 880 Kev است، تجزیه می گردد.
در نتیجه تجزیه و تخریب بتائی نیز اشعه های گاما با انرژی های 724 و 757 KeV ساطع می گردد.
در مورد حادثه چرنوبیل اشعه های ساطع شده گاما مقدار زیادی تابش بسیار بالای گاما را در منطقه اطراف چرنوبیل پراکنده نمودند.
این اشعه ها بصورت ماکسیمم 5 میلی گری (5 milligray h-1) در ماه مه 1986 بود که باعث گردید گونه های درختی زیادی از قبیل کاج در منطقه از بین برود.
غلظت های کریستال طبیعی Zr پایدار (غیر رادیواکتیو nonradioactive) بنحو اجاب انگیزی بالا است.
بوون (Bowen) در سال 1977 اعلام نمود که غلظت های Zr در خاکها در محدوده از 400 تا 2000 میلی گرم در کیلوگرم(mgkg-1) با غلظت میانگین 400 میلی گرم در کیلوگرم است.
غلظت ها در بافت های گیاهی بنحو قابل ملاحظه ئی پائین بود و در محدوده ائی از 0.2 تا 5.0 میلی گرم در کیلوگرم در طیف وسیعی از گیاهان فتوسینتتیک و قارچ ها قرار داشت.Bowen1966
Zr دارای والانس چندگانه (polyvalent)است ولی فقط در حالت والانس 4+ در محیط زیست های آبی قابل مشاهده میباشد.
زیرکونیوم چند والانسی بطور معمول و همراه با سایر عناصر چند والانسی دیگر بسرعت و نسبتاً شدید جذب سطحی خاکها و رسوبات می گردد.
Zrنسبتاً در سیستم های بیولوژیک محیط زیست خاکی از جذب سطحی ضعیفی برخوردار است.
ضرایب توزیع فاز جامد – مایع برایZr95 توسط شیپارد و تی بلوت (Sheppard & Thibault) 1990 در محدوده ئی از 600 لیتر در کیلوگرم (600LKg-1) برای خاکهای ماسه ای و 7300 لیتر بر کیلو گرم(7300LKg-1) برای خاکهای ارگانیک بیان شده است.
فاکتورهای انتقال خاک – گیاه برای Zr95 نادر هستند. ان جی و دیگران در سال 1982 (Ng etal) عدد مورد انتظار را یک هزارم اعلام کردند.
در هر صورت فاکتورهای انتقال ویژه توسط کفتری و تورن (Coughtrey&Thorne) 1983 از 0.006 تا 0.002 برای علف بروموس رابینز (Bromus rubens) و 0.0013 تا 0.004 برای انواع لپه و 0.012 برایپوشال گندم بیان شده است.
میزان و مقدار موثر بکار رفته در واحد جذب بدنبال فرو بردن Zr95 (قورت دادن) ،9.5 X 10-10 Sv Bq-1 برای جوانان بالای 17 سال سن می باشد.(IAEA 1996)
در هر صورت ، اثر محیط زیستی اصلی Zr95 بدلیل نیمه عمر فیزیکی نسبتاً کوتاه آن که ناشی از پرتووش خارجی Zrاست، نسبتاً کوتاه میباشد.
نیوبیوم (Niobium): با عدد اتمی 41 (93Nb)
نام اصلی این فلز رادیواکتیو در واقع کلمبیوم است.(Cb) که در زمان کشف عنصر 41 در سال 1801 به آن داده شد.
ولی اتحادیه بین المللی IUPACدر سال 1949، کلمبیوم رابه نیوبیوم تغییر داد. البته امروزه هنوز کلمبیوم در معدن کاوی و متالوژی استفاده می شود.
نیوبیوم فقط یک ایزوتوپ پایدار بنام 93Nb دارد و دارای 11 ایزوتوپ رادیواکتیو می باشد.
یکی از این ایزوتوپها بنام Nb95 از اهمیت محیط زیستی برخوردار است.
Nb95 دارای نیمه عمر 34.98 روز است و توسط شکافت هسته ئی، فعال سازی نوترونی
و تخریب بتا شکل ، Zr 95ایجاد می شود.
Nb95 توسط تابش های بتا به Mo95 همراه با اشعه های گاما و انرژی های 753 و 768 کلوین ولت (KeV) متلاشی می گردد.
ماکسیمم انرژیNb 95 ناشی از تابش بتا 165 کلوین ولت است.
منابع اصلیNb 95 همانندZr 95 است این منابع عبارتند از: آزمایشات جنگ افزارهای هسته ئی، پسماندهای رادیواکتیو و انفجارات حاصل از نیروگاه هسته ئی چرنوبیل.(Chernobyl)
برواو و دیگران (Boroui etal) در سال 1988 محاسبه کردند که فعالیت ویژهNb95 دست پخت راکتور چرنوبیل (Chernobyl) در زمان حادثه 3.4 X 1010 Bq g-1 بوده است.
و همانندZr 95 اشعه های گاما بسیار بالائی در نزدیکی راکتور چرنوبیل (Chernobyl) تولید کرده است.
این مطلب توسط کنوپلو و دیگران در سال 1993 نیز تائید شده است.
لذNbا 95 علی رغم کوتاه بودن نیمه عمر فیزیکی به میزان زیادی اشعه گاما در اطراف نیروگاه هسته ئی چرنوبیل پراکنده نموده است.
غلظت های محیط زیستی نیوبیوم پایدار (غیر رادیو اکتیو) کمتر از Zr است .(زیرکونیوم)
محدوده آن از 6 تا 300 میلی گرم در کیلوگرم در خاکها و غلظت های 0.3 میلی گرم در کیلوگرم (mg kg-1) در درختان چوبی یافت شده است.
بوون (Bowen) در سال 1979 نیوبیوم به لحاظ شیمیائی و فیزیکی نظیر تان تالم TANTALUMاست .
حالت های والانس چهار ظرفیتی از 2+، 3+، 4+ و 5+ است . ا نتظار می رود این عنصر چهار والانسی در خاکها و رسوبات از جذب سطحی بسیار قوی برخوردار باشد.
در هر صورت دامنه ضرایب توزیع جامد – مایع برای خاکها کمتر از Zr95 است. شپارد و تیبالد (Sheppard & Thibauld) در سال 1990 اعلام کردند که اوزان Kd برای نوبینوم (Nb95) در محدوده ئی از 160 L kg-1 برای خاکهای ماسه ئی تا 2000 L kg-1برای خاکهای ارگانیک است.
این اوزان(Kd) نیز به اندازه کافی بالا بوده و در نتیجه جذب بیولوژیکی بالقوه Nb95 را محدود نمی کند.
فاکتورهای خاک به گیاه برای Nb95 بخوبی مورد مطالعه قرار نگرفته است.
بدین ترتیب به نظر می رسد که تجمع Nb95 در گیاهان قدری بیشتر از Zr95 باشد.
نوبینیومبصورت مقایسه ئی نسبت به زیرکونیوم در انواع خاکها از جذب سطحی پائین تری برخوردار است.
مقدار و میزان موثر Nb در هر واحد جذب بدنبال بلعش Nb95 مساوی 5.8 X 1010 SvBq-1 برای بالغین بیشتر از 17 سال سن است.
نیمه عمر کوتاه Nb95 بدین معنی است که اثر اصلی محیط زیستی آن که ناشی از پرتوش های خارجی است کوتاه می باشد.
وتا حدود بسیار زیادی همانند Zr95 است. (IAEA 1996)
تکنتیوم (Technetium): با عدد اتمی 43(Tc)
Tc یک فلز گذار است. (ترانزیت)
در تمام حالتهای اکسیداسیون بین 7+ و 1- موجود می باشد، همه ایزوتوپهای آن رادیواکتیو بوده و فقط یکی از آنها یعنی Tc99 در نتیجه شکافت خود انگیختهU 238 (اورانیوم 238) بصورت طبیعی موجود است.
در هر صورت منابع اصلی Tc در محیط زیست مصنوعی و ساختگی بوده و ایزوتوپی که بیشترین نگرانی ها را در محیط زیست ایجاد می کند Tc99 است.
این موضوع بخاطر فراوانی و نیمه عمر طولانی آن است. (4.2 X 106 سال) منابع Tc99 در محیط زیست توسط دسمیت و میتینایر Desmet & Myttenacre ) و بنت و والی(Bennett & Willey) در سالهای 1986 و 2003 بررسی و بازنگری گردیده اند.
Tc در اشکال فرار و آبی (محلول آبی)،آزاد می گردد و در هر دو حالت فوق Tc با خاک هوادهی شده ، ارتباط پیدا کرده و در شکل آنیون در پرتکنتیت (Pertechnetate Tc O4-) بصورت محلول غالب است.
آنیون فوق واکنش ناچیزی با ترکیبات خاک دارد و لذا فرض بر این است که تحرک و جابجائی بالائی در خاک داشته باشد.
بعلاوه Tc بسهولت جذب گیاهان و میکرواورگانسیم ها می گردد و جذب آن در محلول توسط آنیون ها کاهش می یابد.
آنیونهای کاهنده Tcعبارتند از:
NO3-, H2PO4-, SO42- و MoO42-
کاتالدو و دیگران (Cataldo etal) در سال 1983 و اچواریا و دیگران (Echevarria etal) در سال 1998 علائم مسمومیت شیمیائی Tc راغالباً گزارش کرده اند و اغلب با پروتئین ها در گیاهان که احتمالاً جانشین S در لیگاندهای تیو می گردد، همراه است.
حالت اکسیداسیون غالب Tc در محلول آبی 7+ است.
Tc در پرتیکنیتات (Pertechnetate) یک اکسیدانت ضعیف است.
Tc در محدوده وسیع از PH و غلظت ،پایدار است.
(VII)Tc توسط مواد ارگانیک و عاملهای کاهنده مختلفی همچون هیدرواکسیدان و اسید اسکوروبیک (hydroxylamine & ascorbic acid) به (Vi)Tc تبدیل می گردد.
اشکال آبی (Vi)Tc ممکن است مجدداً به (VII)Tc به درجات متفاوتی توسط هوا ، H2O2 , HNO3, MnO4-, Cl2 مجدداً اکسیده گردد.
شیمی Tc در خاک نسبت به محلول آبی آن پیچیده تر است.
پرتکنتیت در شرایط هوازی یا هوادهی غالب است. این آنیون همانند نیترات فقط بصورت خیلی محدود توسط ترکیبات خاک جذب سطحی می گردد.
به نظر می رسد که از تحرک و جابجلئی قابل ملاحظه ئی برخوردار باشد.
در حقیقت ضریب توزیع Kd معمولاً نزدیک صفر است.
باچ هوبر و دیگران (Bachhuber etal) در سال 1986اعلام کردند که Tc بعنوان پرتکنتیت که به خاکها اضافه می شود، حرکت محلولی قابل ملاحظه ئی از خود نشان می دهد. و به سهولت جذب ریشه های گیاهان می گردد. اچواریا و دیگران (Echevarria etal) در سال 1986 بیان نمودند که Tc حتی تحت شرایط اکسیده شدن قابل حل نبوده و انتظار می رود بعنوان یک آنیون تک والانسی ساده از تحرک بیشتری برخوردار باشد.
اسچیماک و دیگران (Schimmack etal) در سال 1993 نشان دادند که Tc95m در خاک جنگلی ارگانیک نسبت به برومید (bromide) از جابجائی وتحرک عمودی کمتری برخوردار است. ولدانگ و دیگران (wildung etal) در سال 1974 پیدا کردند که جذب سطحی Tc95m اگر چه خیلی کم، بصورت مستقیم با محتوای مواد ارگانیک خاک همبستگی دارد.
اگر چه با PH این نسبت بر عکس می شود، این وضعیت دلالت بر این موضوع دارد که نقش مواد ارگانیک و احتمالاً آهن و اکسیدهای آلومینیم برجسته است.
شیپارد و دیگران (Sheppard etal) در سال 1990 گزارش کردند که جذب سطحی Tc95m با افزایش محتوای ارگانیک خاکها، افزایش می یابد.
مطالعات اخیر نشان داده است که Tc(VII) با مواد ارگانیک مخصوصاً اسیدهای هیومیک همراه است و توسط واکنش های اکسیداسیون و احیاء معادلات فوق صورت می پذیرد. میس و دیگران (maes etal) در سال 2003
در یک اظهار نظر جدی می توانیم بیان کنیم که تمامی واکنشها و معادلات فوق، بدلیل اینکه واکنش های جذب سطحی نمی باشد، ممکن است به لحاظ آزمایشکاهی تشخیص جذب سطحی و واکنش مشکل شود.
در نهایت نتیجه قطعی واکنش های فوق حذف Tc از محلول است.
به هر حال حتی اشکال قابل حل Tc ممکن است با ترکیبات ارگانیک توده مولکولی پائینی همراه باشد.
این ترکیبات پیچیده برای جذب توسط ریشه ها نسبت به آنیون پرتکنتیت آبی، کمتر در دسترس باشد. یانگیساوا و دیگران (Yangisawa etal) در سال 1997
بی تحرک سازی و عدم جابجائی Tc در شرایط کاهنده، برجسته تر است.
در حدود 98% Tc، هنگامیکه خاکها در بطری های پلمپ شده و در بسته قرار داده می شوند از محلول حذف می گردند. لاندا و دیگران (Landa etal) در سال 1977
شپارد و دیگران (Sheppard etal) در سال 1990، اوزان Kd بسیار بزرگتری برای خاکهای غیر هوازی نسبت به خاکهای هوازی پیدا کردند.
در مقابل در حدود 40% Tc در رسوبات آبی دره ئی ،بدون اکسیژن بصورت محلول باقی می ماند.
کیت – روچ و روس (Keith – Rouch & Roos) در سال 2004، یانگیساوا و موراماسو (Yangisawa & Muramasu) در سال 1995 گزارش کردند که Tc(VII) همراه با زمان و تحت شرایط کاهنده و هوادهی کم تبدیل به اشکال غیر قابل حل Tc(VI) می گردد.
Tc در دو نوع خاک در طول یک دوره شش ماهه در شرایط غیرهوازی بی تحرک می گردد، ولی نه هنگامیکه دو خاک فوق در شرایط هوازی نگه داشته شوند. تاگامی و آچیدا(Tagami & Uchida) در سال 1999 گزارش دادند که حلالیت Tc در خاکهای آغشته به آب در طول یک دوره 52 روزه به تدریج کاهش می یابد.
هنگامیکه خاک با هوا خشک گردد یا در شرایط هوازی قرار گیرد، Tc بسیار کمی مجدداً به تحرک واداشته می شود.
مطمناً فعالیت میکروبی در بی تحرک سازی Tc مشارکت جدی دارد و این موضوع بخاطر تاثیر آن بر شرایط اکسیداسیون و احیاء است.
ولی دانشمندان شواهد نتیجه بخشی از اثر مستقیم در خصوص اینکه بی تحرک سازی Tc بخاطر جذب سطحی میکروبی باشد، پیدا نکرده اند. تاگامی و آچیدا (Tagami & Uchida) در سال 1996 و اخیراً آشورت و شائو (Ashworth & Shaw) در سال 2005 گزارش کرده اند که Tc بکار رفته در ستونهای خاک پایه به نظر می رسد که در نزدیکی چشمه آب اشباع شده ، جائیکه شرایط کاهنده باشد، باقی می ماند.
آنها نتیجه گرفته اند که پرتکنتیت بصورت جزئی به Tc(IV) تبدیل گردیده است و به آرامی بسوی ستون خاک حرکت می کند.
چندین مطالعه دیگر برای شناسائی اشکال قابل حل جزئی Tc در خاک نیز انجام شده است. کیت – روچ و دیگران(Keith – Rouch etal) در سال 2003 روشی برای جذب Tc که عبارت بود از طرح جداسازی متوالی شیمیائی را مورد استفاده قرار دادند.
آنها فراکسیون های (Fractionations) متفاوتی برای سه رسوب مطالعه شده پیدا کردند. در یک مورد بخشی اصلی به کربنات ها نسبت داده شده است.
به هر تقدیر دانشمندان در جستجوی این حرکت بودند که ممکن است سولفید (Sulfide) نیز توسط عصاره استات اسیدی حل گردد.
وال مان و دیگران (Wallman etal) در سال 1993 و نهایتاً عبد لوس و دیگران (Abdelouas etal) در سال 2005 نتیجه گیری کردند که اغلب Tc غیر محلول در خاکهائیکه از مواد ارگانیک قوی هستند بعد از نهفتگی بدون اکسیژن با مواد ارگانیک همراه می شوند و تقریباً 60 تا 66 درصد Tc توسط پراکسیدهیدروژن قابل استخراج است.
بخش قابل ملاحظه ائی تقریباً 21 تا 23 درصد با اکسی هیدرواکسیدهای آهن (Fe-Oxyhdroxides) همراه بوده و توسط هیدرواکسیلامین (Hydroxylamine) قابل استخراج است.
دستگاه اسپکتروسکوپی جذب سطحی اکس ری (X- ray adsorption spectroscopy) تائید کرده است که نوع Tc غیر قابل حل شکل گرفته در رسوبات کم اکسیژنه در واقع هیدراته TcO2 است. بورک و دیگران (hydrous TcO2 Burke etal) در سال 2005
نقش دقیق میکروارگانیسم ها در کاهش Tc بنحو گسترده ئی در کشت میکروبی یا در محلول، بیشتر از خاک، مورد مطالعه قرار گرفته است.
جذب زیستی پرتکنیتات (Biosorption of pertechnetate) توسط باکتری های سیان (Cyanobacteria) وابسته به انرژی نبوده و به راحتی برگشت پذیر است. مضافاً اینکه کاهش Tc را هم بدنبال ندارد.
گارن هام و دیگران (Garnham etal) در سال 1993
به هر ترتیب سایر باکتری های با ظرفیت مشخص کاهندگی فلزات قادرند که Tc(VII) را به Tc(IV) تبدیل کنند. و در مواقعی نیز آنرا به Tc(V) تبدیل می کنند.
کاهش کاتابولیت فلزات در محیط های کم اکسیژن توسط لولی (Lovley) بخوبی در سال 1993 مورد مطالعه قرار گرفته است.
این مطالعه در دهه گذشته با تکیه بر آهن، منگنز، کروم، اورانیوم، آرسن و سلینیوم صورت گرفته است.
در ضمن باکتری های کاهنده سولفور مختلفی(Various sulfur – reducing bacteria) از قبیل Shewanella putrefaciens ، Geobacter metallireducens ، G Sulfurreducens و
Desulfovibrio dessulforicans گزارش شده است که Tc(VII) را تحت شرایط غیر هوازی کاهش می دهند.
این مطالب را دانشمندان متعددی از قبیل عبدلوس و دیگران ، بورکی و دیگران (Abdelouas etal , Burke etal) بترتیب در سالهای 2002 ، 2005 و 2005 گزارش کرده اند.
اسچیریا کولی (Escherichia coli) تحت شرایط غیر هوازی و کلستری دیا (Clostridia) که باکتری های تخمیری کاملاً غیر هوازی هستند نیز گزارش شده است که کاهنده Tc و رسوب دادن آن می باشد.
باکتری های گرم منفی (Gram – negative bacteria) ممکن است Tc را تحت شرایط اکسیدی به اشکال غیر قابل حلی، انتقال دهند.
نشانه بخصوصی از اینکه باکتری نیتروژن زدای اختیاری (Facultative denitrifying bacteria) و هوازی بتواند Tc را کاهش دهد وجود ندارد.
البته در بعضی مطالعات دو مکانیزم متمایز کاهش Tc تشخیص داده شده است.
این مکانیزمها عبارتند از:
1- کاهش آنزیمی مستقیم.
2- مکانیزم های غیرمستقیم.
که توسط ترکیبات پرتاب دهنده الکترونی (شاتل) تسریع می گردد.
شامل آنالوگهای هوموسی (Humic) (مواد آلی) که در بعضی مواقع توسط ترسیب روی مواد بیولوژیک شکل گرفته تازه، دنبال می شود.
عبدولوس و دیگران (Abdelouas etal) در سال 2002 با استفاده ازالکترون دهنده های مختلف واکنش های فوق مورد استفاده بررسی قرار دادند که کاراترین آنها فرمات (Formate) و پیرووات (Pyruvate) می باشند.
به نظر می رسد کاهش Tc در زمان کاهش Fe(III) فعال اتفاق می افتد و قبل از کاهش سولفات تکمیل می گردد. بورک و دیگران (Burke etal) 2005.
تا به امروز شواهدی از کاهش میکروبی به شکل متیل شده فرار Tc مشاهده نشده است.
لذابه نظر می رسد برای Tc،سلینیوم و سایر فلزات مختلف کاهش میکروبی وجود نداشته باشد.
روتنیوم (Ruthenium): با عدد اتمی 44 (Ru)
عتصر روتنیوم دارای 7 ایزوتوپ پایدار است.
این ایزوتوپها عبارتند از:
،104Ru102Ru، 101Ru، 100Ru، 99Ru، 98Ru، Ru96
از ایزوتوپهای فوق 102Ru دارای بیشترین فراوانی است.(تقریباً 32 درصد)
این عنصر نیز 5 ایزوتوپ رادیواکتیو می باشد که عبارتند از:
106Ru، Ru105 Ru103، 97Ru، 94Ru کهRu 103 و Ru106 از نظر آلاینده های محیط زیستی حائز اهمیت می باشند.
103 Ru بواسطه شکافت هسته ئی و فعال سازی نوترونی،Ru 102 شکل می گیرد. در صورتیکه 106Ru صرفاًدر نتیجه شکافت هسته ئی بوجود می آید.
نیمه عمر هایRu 103 و Ru106 بترتیب 39.26 و 373.6روز است که هر دو ایزوتوپ رادیواکتیو این عنصر در نتیجه رهاسازی های جنگ افزارهای هسته ئی و طرح های برنامه ریزی شده و همچنین عملیات تصادفی (انفجارات) از نیروگاه های هسته ئی وارد محیط زیست می گردند.
تمام فعالیت های دپو شده (انبار شده) Ru 106 در سه کیلومتری ناحیه انفجار چرنوبیل در محدوده0.1 تا 1.02MBqm-2 تعیین شده است. وانک (Wang) 1996
البته مقدار واقعی رها شده به مکان بستگی دارد.(دوری و تزدیکی از مکان حادثه) کروگلو و دیگران (Krouglov etal) 1998 گزارش دادند که کل میزان فعالیت های رادیواکتیوته 106Ru در 30 کیلومتری منطقه انفجاری چرنوبیل از1.2 تا9.2 MBqm-2 در نوسان است.
بیشتر روتنیوم رهاشده احتمالاً همراه با بخشهای از سوخت راکتور (ذرات داغ) در چند ده کیلومتری اطراف چرنوبیل پراکنده شده است.
در هر صورت رونیو و دیگران (Ronneau etal) در سال 1995 گزارش کردند که تقریباً 100 درصد روتنیوم در یک ماتریس اکسید اورانیوم در هنگامی که درجه حرارت بالا باشد، در زمان آتش گرفتن راکتور می تواند تبخیر گردد.
106Ru در خاکهای در اروپا غربی و اسکاندیناویا (Western Europe and Scandinavia) در هفته های اولیه به دنبال انفجار چرنوبیل (Chernobyl) باید از طریق اتمسفر و در شکل آئروسل انتقال یافته باشد.
شکل فیزیکی ، شیمیائی 106 Ru که در سطوح خاک در مناطق نزدیک و خیلی دور دپوزیت (deposite) شده است، کاملاً متفاوت بوده است.
در حقیقت اطلاعات در خصوص غلظت های طبیعی روتنیوم پایدار در مواد محیط زیستی (Environmental materials) ناکافی و بسیار محدود است.
البته اطلاعاتی به ندرت پیدا می شود که اوزان 0.01Mgkg-1 برای صخره های آذرین (آتشین) گزارش شده است. بوون (Bowen) 1996
اوزان و اندازه گیری های روتنیوم پایدار در بافت های گیاهی نیز نادر است. البته بوون اوزان 0.005 mgkg-1 در آنجیواسپرمها (angiosperms) که 5 برابر میزان موجود صخره های آذرین است را نیز پیشهاد داده است.
روتنیوم ساختار شیمیائی پیچیده ئی داشته و حالت های والانسی آن هفت تائی است.(seven valence state)
اگر چه والانس های 2+ ، 3+ و 4+ بیشتر یافت می شوند. اسینگ تون و دیگران(Essington etal) در سال 1963 تعیین کردند که حالت های اکسیداسیون 3+ و 4+ در شرایط اسیدی بودن خاک غالب می باشند.
شولتز (schults) در سال 1965 پیشنهاد کرد که به نظر می رسد روتنیوم در کمپلکسیونهای (Complexes) نیتروسیل (nitrosyl) در خاک، نسبت به اشکال ساده تر آن از تحرک بیشتری برخوردار باشد.
البته جونز (Jones) در سال 1960 در نتیجه تحقیقات اعلام کرد که روتنیوم نیتروسیل می تواند با لایه های سطحی ،پوششهای هیدرواکسید آهن در ذرات رسوبی آبی وارد واکنش شده و تشکیل کمپلکسونهای نامحدود بدهد.
در هر صورت لیونس و باکستی (Livens & Baxte) در سال 1988 اعلام کردند که Ru106 بصورت بسیار ضعیفی در خاکهای شمال غربی انگلستان با فاز اکسیده همراه است.
دو دانشمند فوق نیز اعلام کردند که روتنیوم در خاک ها همخوانی بالائی برای چسبیدن به مواد ارگانیک دارد و 30% آن (106Ru) با مواد ارگانیک در خاکهای ماسه ئی یافت می شود.
در حقیقت خاکی که کل محتوای کربن ارگانیک آن فقط سه درصد بود، 30% روتنیوم به آن چسبیده بود.
اندرسن و رود (Anderson & Roud) در سال 1994 اعلام کردند که 70% روتنیوم 106 ناشی از انفجار چرنوبیل در خاک جنگلهای سوئد (Swedis) با مواد ارگانیک همراه بود و مابقی آن حتی 7M HNO3 قابل عصاره گیری نبود.
در هر صورت Ru106علی رغم تمایل واضح برای جذب شدن به مواد ارگانیک خاک، به نحو قابل ملاحظه ئی سریعتر
از 137 Cs و 134 Cs در پروفیل خاک تحرک دارد.
با توجه به مطالعات بالا می توان نتیجه گرفت که ضرایب توزیع Ru 103 و Ru106 در فاز جامد – مایع در خاکهای ارگانیک در بالاترین مرتبه قرار دارد.
شپارد و تیبالت (Sheppard & Thibault) در سال 1990 پیشنهاد کردند که میانگین Kd از 660 LKg-1 با احتمال محدوده 3600 تا120000 LKg-1 برای خاکهای ارگانیک است.
این موضوع با میانگین اوزان 55990Kd و 400LKg-1 برای خاکهای ماسه ئی، لومی و گلی است.
در هر صورت اطلاعات محدودی در خصوص فاکتورهای انتقال خاک – گیاه برای Ru103 و 106 انتشار یافته است.
گسترده ترین منبع فاکتور انتقال خاک – گیاه بر پایه اطلاعات اتحادیه بین المللی رادیواکولوژیست ها (IUR 1989) است.
اگر چه حتی این منبع فقط 17 وزن آزمایشگاهی برای تعداد کمی از محصولات را در بر می گیرد.
این اوزان دارای محدوده ئی از 0.005 تا 1.45 است که وزن میانگین 0.231 می باشد.
ان جی و دیگران (Ng etal) در سال 1982 توصیه کردند که حامل انتقال خاک – گیاه برای ایزوتوپهای روتنیوم 0.04 است.
کفتری و تورن (Coughtrey & Thorne) بر اساس مطالعات متنوعی که در دهه های 1960 و 1970 انجام دادند در سال 1983 اعلام کردند که عاملهای انتقال 0.3 برای کمپلکسونهای روتنیوم نیتروسیل (nitrosyl Ruthenium Complexes) از 0.01 تا 0.1 برای اشکال غیر کمپلکسیون(ساده) روتنیوم است.
ویلی و فات (Willy & Fawcett) در سال 2006 بر اساس اطلاعات بدست آمده اعلام کردند که جذب رتنیوم توسط گیاهان با غلظت های Ru106 ,103Ru و در 113 گونه گیاهی گلدار ، مورد بحث قرار گرفته است.
آنالیزهای آماری نشان داد که تقریباً 2500 مرتبه تفاوت در درجه ئی که گروه های گیاهی متفاوت روتنیوم را جذب می کنند وجود دارد و 36% این تفاوت ها مربوط به تفاوت های طبقه بندی در گیاهان است.
بدین ترتیب مشخص گردید که گیاهان متفاوت، جذب متفاوتی از روتنیوم دارند و مقدار موثر بدست آمده در هر واحد جذب در نتیجه بلعش و حذف Ru106 ،103و به ترتیب 7.3X10-1 و 7.0X10-9SvBq-1 برای افراد بالاتر از 17 سال سن است.
(IAEA 1996)
نقره : (Silver) با عدد اتمی 47 (Ag)
نقره در طبیعت به شکل دو ایزوتوپ پایدار وجود دارد که(51.4%)107Ag و 109Ag(48.6%) درصد را بخود اختصاص می دهند.
این فلز رادیواکتیو دارای 12 رادیونیوکلید است که 108mAg , 110mAg و 111Ag ممکن است در نتیجه چرخه سوخت هسته ئی، اشعه ساطع کنند .
از آنجائیکه در اثر انفجار چرنوبیل110mAg، در سال 1986 ساطع گردید، از نظر آلایندگی محیط زیستی بیشترین توجه را به خود جلب کرده است.
اشعه ساطع شده از نقره در جریان حادثه فوق در فاصله 2000 کیلومتری غرب راکتور در اکوسیستم ها توسط برسفورد (Bersford) در سال 1989a کشف گردید.
بر اساس تحقیقات مشخص گردید که اشعه این فلز در کبدهای حیوانات و گونه های قارچی گیاهی تغلیظ می گردد. 110mAg دارای نیمه عمر 249.8 روز است.
(LBNL پروژه ایزوتوپها (isotopes projects) 2004).
110Ag توسط فعال سازی نوترون 109Ag تولید گشته و بواسطه تابش های بتا(β) به کادمیم 110 تجزیه می گردد.
در جریان تابش، طیفی وسیعی از اشعه های گاما در محدوده KeV 450 تا 1560 نیز تولید می گردد.
غلظت های طبیعی نقره پایدار در خاکها، محدوده ئی از 0.01 تا 8 mg kg-1 است. این مطلب را بوون (Bowen) در سال 1979 بیان کرده است.
نقره از جمله واکنش پذیرترین فلزات نادر (noble) است و دارای سه کاتیون بنام های Ag+، Ag2+ و Ag3+ است و محاسبات تعادل شیمیائی آن توسط لیندسی (Lindsay) در سال 1974 انجام گرفته است.
دانشمند فوق اعلام نمود که به نظر می رسد فقط Ag0 و Ag+ در خاکها از اهمیت ویژه ئی برخوردار باشد.
پتانسیل اکسیداسیون و احیاء و PH عاملهای کنترلی بحرانی در ارتباط با رفتار نقره در انواع خاکها و تحت شرایط کاهنده قلمداد می گردد و در چنین حالتی رسوب Ag در شکل AgS محتمل است. لیپ و دیگران (Lepp et al) در سال 1995.
نقره در لایه های بالای خاک بواسطه واکنش با مواد ارگانیک خاک بی تحرک می گردد.
بر طبق نظر Lepp,etal ،Ag پیوند خورده با مواد ارگانیک بخش قابل ملاحظه ئی از کل ترکیب نقره (Ag ) بوده و نقش بسیار مهمی در کنترل چرخه نقره در خاک دارد.
حرکت و رفتار نقره (Ag ) نیز در خاکها اثر قابل ملاحظه ئی بر چرخه آن دارد.
اثر رفتار دراز مدت نقره در خاک که محتوای کربن ارگانیک آن 6.8% است نیزمطالعه گردیده است.
حرکت رو به پائین Ag لز سطح خاک بسیار کند بوده و نصف زمان ماند آن برای لایه خاک 5 سانتی متری در سطح 33 سال است.
این مهم بدین معنی است که Ag 110m قبل از هر گونه حرکت قابل ملاحظه و نشت در خاک تقریباً بصورت کاملی تحت تجزیه و تخریب فیزیکی واقع می گردد.
توزیع جامد – مایع Ag و جابجائی آن در خاکها نیز مخصوصاً خاکهای که کربن ارگانیک قابل ملاحظه ائی دارند، محدود است.
بهترین تخمین اوزان کاری برای خاکهای ماسه ئی، گل و لای و لوم و ارگانیک بترتیب 90، 180، 120 و 1500، LKg-1 است.
محدوده تخمین های Kd برای خاکهای ارگانیک 2400 تا 89000 ، L Kg-1 است.
هاندل و دیگران (Hndl etal) در سال 2000،
عاملهای انتقال اندازه گیری شده Ag را در علف های مرتع در محدوده از 0.009 تا 0.065 گزارش کرده اند.
این محدوده کمی بیشتر از فاکتورهای انتقال خاک – گیاه که بصورت محدود در کاهو با عدد 0.00027 وبرای گوجه فرنگی0.0008 و برای هویج 0.0013جمع آوری شده است می باشد.
ان جی و دیگران (Ng et al) در سال 1982 اعلام کردند که فاکتور انتقال با ارزش 0.15 برای Ag در نقاط گیاهی نامشخص محتمل است.
مقدار موثر بدست آمده در هر واحد جذب در نتیجه بلعش 110mAgبرای افراد بزرگتر از 17 سال 2.8X10-9 SvBq-1 گزارش شده است. IAEA در سال 1996
آنتیمونی (Antimony): با عدد اتمی 51 (Sb)
دو ایزوتوپ پایدار آنتموان (Sb) بنام های 121Sb (57.2%) و 123Sb (42.8%) بصورت طبیعی موجود هستند.
Sb دارای 20 رادیو نیوکلید است.
ولی نگرانی عمده محیط زیستی در واقع 125Sd است که نیمه عمر آن 2.76 سال می باشد.
125Sd یک محصول شکافت هسته ئی است. و نیز بواسطه فعال سازی نیترون 124Sn که برای تولید Sn 125(قلع) بکار می رود تولید می شود که با نیمه عمر 9.7 دقیقه به Sn 125و مطابق آن Te 125متلاشی می گردد.
Sb 125(آنتمونی 125) بواسطه تابش بتا تجزیه می گردد و همچنین محدوده ئی از اشعه های گاما را نیز تولید می کند.
از میان اشعه های تولید شده، اشعه اصلی در 427KeV (30.6%) و 598KeV (18.6%) می باشد.
آنتمونی یک شبه فلز بوده و شباهت های شیمیائی با آرسینک (Arsenic) دارد. ولی کمتر از آرسن در محیط طبیعی موجود است.
بوون (Bowen) در سال 1979 گزارش کرد که دامنه ئی از غلظت های Sb از 0.2 تا (mg kg-1) 10در خاکها وجود دارد. و عدد میانگین آن یک میلی گرم در کیلوگرم است. کفتری و دیگران (Coughtrey etal) در سال 1983.
کل محدوده های غلظت Sb در خاکها از 0.05 تا (mg kg-1) 260است.
دانشمندان فوق در همان سال توضیح دادند که میانگین جهانی غلظت نسبی در خاکها(یک میلی گرم در کیلو گرم) در واقع فاکتوری که بیشتر از میانگین جهانی غلظت Sb در پوسته قشر زمین است. یعنی 0.2 میلی گرم در کیلوگرم است.
بنابراین Sb در خاک نسبت به مواد مادر متراکم می شود. افزایش با منشاء انسانی (Anthropogenic enhancement) غلظت های Sb در محیط زیست معمولاً مرتبط با فعالیت های صنعتی از قبیل معدن کاوی و فلز کاری است.
البته بکار گیری روشهای تصحیح خاک از قبیل کودهای سوپر فسفات و خاک و سوزاندن ذغال تا 20 میلی گرم در کیلوگرم موجب افزایش غلظت Sb می گردند.
لیپ و دیگران (Lepp et al) در سال 1995
آنتمونی همانند آرسنیک می تواند در حالت های اکسیداسیون (Antimonite) 3+ و (Antimonate) 5+ وجود داشته باشد.
ولی Sb3+ ساده و Sb5+ کاتیون ها به نظر نمی رسد که بصورت محلول وجود داشته باشند.
پیترسون و گریلینگ (Peterson & Grilling) در سال 1981 اعلام کردند که احتمالاً آنتمونی در خاکها عمدتاً بصورت آنتمونات (antimonate SbO3-) وجود داشته باشد.
فونت و دیگران (Fuents et al) در سال 2003 تائید کردن که معمول ترین گونه های عصاره گیری شده خاک Sb است.
بودک و دیگران (Bodek et al) در سال 1988 اعلام کردند که اشکال هیدرولیزه Sb احتمالاً در محلول بیشتر است.
در خاکهای اکسیک(Oxic) در -pH > 3.0, sb(OH)6 احتمالاً غالب باشد.
در صورتیکه در شرایط اکسیداسیون و احیاء پائین، Sb(OH)3 به نظر غالب می آید.
کاباتا پندیاس و پندیاس (Kabata – pendias & pendias) در سال 1984، آنتی مونی (antimony) را بعنوان یک شبه فلز که بصورت آرام و معتدل در خاک جابجا می شود طبقه بندی کردند.
این طبقه بندی نیز توسط دی سوزا و میس تری (D,souza & mistry) در سال 1980 تائید گردید.
دو دانشمند فوق به این نتیجه رسیدند که Sb 125بکار رفته در سطح خاک تحت شرایط حاره ئی در فاصله زمانی 33 ماه در عمق 10 سانتی متری خاک پائین می رود. بدین ترتیب مشاهده فوق بنحو مطلوبی با اوزان Kd منتشر شده برای Sb در طبقات خاک جنریک (generic) سازگاری دارد.
این محدوده ها از 45LKg-1 در ماسه ها تا ماکسیمم 540LKg-1 در خاکهای ارگانیک قرار دارد.
ناکامورا و دیگران (Nakamura et al) در سال 2005 گزارش کردند که میانگین 62LKg-1 Kd برای Sb 124در خاکهای کشاورزی ژاپن بدست آمده است.
اگر چه ماکسیمم Kd که آنها مشاهده کردند 2065LKg-1 بود.
جذب سطحی Sb در هپاتیت معدنی خاک بنحو گسترده ئی به PH وابسته است.
با افزایش قابل ملاحظه جذب سطحی ،PH تا زیر 7 کاهش می یابد. این جذب سطحی تا حدود بسیار زیادی شبیه گونه های آرسینات (arsenate) است.
ناکامورا و دیگران (Nakamura et al) در سال 2005 تائید کردند که این وابستگی PH در 110 نوع خاکهای کشاورزی ژاپن صحت دارد.
آنها برای دو نوع خاک بنام های آندوسول (Andosol) و فلویسول(Fluvisol) تاثیر تنظیم PH را مطالعه نموده و گزارش کرده اند که با کاهش PH به پائین تر از 7 جذب سطحی بصورت لگاریتمی (Logarithmical) افزایش می یابد.
جذب سطحی Sb در خاکها نیز با افزایش غلظت فسفات کاهش می یابد.
غلظت های آنتی مونی در بافت های گیاهی محدوده ئی از 0.0001 تا mg kg-10.2 وزن خشک گزارش شده است. بوون (Bowen) در سال 1979.
میانگین جهانی غلظتSb، یک میلی گرم کیلوگرم (mg kg-1) است.
این وضعیت بدین معنی است که فاکتورهای انتقال خاک – گیاه برای Sb چیزی کمتر از یک است.
بدین ترتیب غلظت های Sb در انواع مختلف گیاهان بر اساس غلظت نرمال Sb در خاک یک میلی گرم در کیلوگرم است.
فاکتورهای انتقال خاک – گیاه برای Sb در سبزیجات طبیعی 0.1، علفهای مرتع 0.05، غلات، حبوبات و سبزیجات علفی 0.05، سیفی جات، سبزیجات ریشه دار و باغهای میوه 0.005 است.
IUR در سال 1989 گزارش کرد که فاکتورهای انتقال توسعه داده شده بر اساس آزمایشات با Sb 125 که ضرورتاً کمتر از اوزان پیشنهاد شده توسط کفتری و دیگران (Coughtrey et al) می باشد .
فکتورهای انتقال برای هویج 5.6X10-4 و برای کاهو 1.3X10-4 و گوجه 8X10-5 اعلام شده است.
ولی اطلاعات IUR در سال 1989فاکتورهای انتقال را کمتر از میزان فوق برای Sb در گیاهان مختلف بیان کرده است.
بعنوان مثال: برای لوبیا 0.4، هویج 1.5 و کاهو 5.8 ذکر شده است.
از طرف دیگر لوکس و دیگران (Lux et al) در سال 1995 فاکتورهای انتقال را برایSb 125 در سزیجات در فاصله 30 کیلومتری چرنوبیل 0.001 تا 0.01 برای Sb 125گزارش کرده اند.
بدین ترتیب آنها نتیجه گرفتند که تجمع رادیونیوکلیدهائی از قبیل Sb 125در گیاهان قابل ملاحظه نمی باشند.
بطور خلاصه به نظر می رسد که عدم قطعیت قابل ملاحظه ئی در خصوص مناسب ترین فاکتور انتقال در رابطه با آنتی مونی وجود دارد.
این موضوع شاید بواسطه تفاوتها در درجه جذب گیاهی Sb پایدار را تشدید کند و Sb 125موجود در خاک در دوران های کاملاً متفاوت نیز شامل این موضوع می گردد.
دوز موثر (مقدار) اختصاص یافته در واحد جذب بدنبال بلعش Sb 125برای افراد بالاتر از 17 سال سن 1.1X10-9 Sv Bq-1 است . IAEA 1996
سزیم با عدد اتمی 55: (Cs)
سزیم یک فلز قلیائی است و ساختار شیمیائی معمولی خیلی ساده ئی دارد. فراوانی طبیعی ایزوتوپ پایدار (133Cs)100% است.
ممکن است که سه عدد از رادیوایزوتوپهای مصنوعی آن در محیط زیست وجود داشته باشد که دو تا از آنها در غلظت های مختلف در بیشتر سیستم های خاک موجود هستند.
134Cs دارای نیمه عمر 2.06 سال است. و نیمه عمر 137Cs، 30.1 سال است.
هر دو ایزوتوپ فوق ترکیبات اصلی هستند که در آزمایشات جنگ افزاری دهه های 1950 و 1960 در اتمسفر پراکنده شدند.
در اطراف نیروگاه هسته ای و تجهیزات مربوط به انبار کردن ذباله های هسته ئی نیز وجود دارد.
ایزوتوپهای نام برده شده فوق نیز در اطراف نیروگاه منفجر شده چرنوبیل در سال 1986 پراکنده شده اند.
135Csکه دارای عمر طولانی در محیط زیست است (سال2.3X106) جز مهمی از ذباله های رادیواکتیو با عمر طولانی است.
بدین ترتیب استراتژی های مدیریت ضایعات هسته ئی باید امکان و احتمال وارد شدن 135Cs را بصورت جدی تحت نظر داشته و مورد بررسی قرار دهند.
البته ایزوتوپ فوق تا به امروز در محیط زیست کشف نشده است.
Cs نقش بیولوژیکی مشخصی ندارد و حداقل در غلظت هائی که پیدا می شود نقش بیولوژیکی آن بسیار کم رنگ است.
سزیم در غلظت های بسیار بالا (Millimolar) فوق العاده سمی است. ایوری(Avery) در سال 1995 و هامتون و دیگران (Hompton et al) در سال 2004 ، تحقیقاتی را در خصوص بستن کانالهای پتاسیم توسط سزیم در غشاء های بیولوژیکی انجام دادند.
علی رغم ظرفیت سیستم های بیولوژیکی برای تمایز بین دو عنصر فوق به نظر رسید که رفتار سزیم بسیار شبیه به K است.(پتاسیم)
شیمی سزیم در خاک بواسطه ویژه گیهای جذب سطحی کمپلکس آن غالب است.
بدین ترتیب سزیم بنحو فزآینده ئی در سطوح معدنی خاک بطرز فوق العاده برگشت ناپذیری بی تحرک است.
مواد ارگانیک سزیم را بصورت انتخابی جذب نمی کنند و نقش مواد ارگانیک در جذب سزیم معمولاً تا حدود بسیار زیادی غیر مستقیم است.
منابع مختلفی برای رادیو سزیم در محیط زیست وجود دارد.
ورود سزیم ناشی از آزمایش جنگ افزارهای اتمسفری در میانه (اواسط) قرن دوازدهم منجر به توضیح گسترده و همگون آلودگی خاک و آب گردید.
سهم الشرکه ی تجمع 137Cs ناشی از محل و منبع آزمایشات جنگ افزارهای اتمسفری در اروپا، 1000Bqm-2 است.ته نشست نسبتاً یکنواخت 137Cs ناشی از پراکنش در نتیجه تست جنگ افزارهای هسته ئی منجر به استفاده گسترده از این ایزوتوپ بعنوان
یک ردیاب فرسایش منجر گردید.ریدچی و مکلنری (Ritchie & Mcllenry) در سال 1990 ، آگودو (Agudo) در سال 1998.
انفجاری که در نیروگاه هسته ئی چرنوبیل در اوریل 1986 بوقع پیوست، منجر به آلودگی محلی بیشتر گردید.
حوادثی که منجر به این اتفاق و پیامدهای آن گردید بنحو گسترده ئی توسط AEN 1987 و ساوچینکو (Savchenko) 1995، آرکورک و دیگران (Arkorg et al) 1999 و IAEA در سال 2001 بنحو گسترده ئی گزارش شده است.
بعنوان مثال: بیشتر از 8.4mha (میلیون هکتار) از سرزمین های کشاورزی در سطح 3.7KBqm-2 یا بیشتر در کشور اکراین آلوده گردیده است.
این میزان در فرانسه کمتر از 1000 تا 10000 الی 12000 Bq-2 در شرق فرانسه و 37000Bq-2 در بعضی از مناطق ، از قبیل کوه های آلپ و پرسیکا با توجه به میزان نزولات جوی در اوایل ماه مه همان سال آلوده گردید.
میزان مشابهی نیز در کشورهای دیگر در اروپای غربی، شرقی و مرکزی مشاهده شده است.
بدلیل الگوهای نزولات جوی و مسیر ابرهای رادیواکتیو بعد از حادثه چرنوبیل، کشورهای OECD بیشترین تاثیر را گرفته اند. کشورهای اسکاندیناوی (Scandinavian) نواحی کوهستانی آلپ و بخش های از جزایر بریتانیا نیز الوده شدند.
الگوی نامنظم پراکنش اشعه های ناشی از انفجار چرنوبیل، استفاده از 137Cs را بعنوان یک ردیاب برای افزایش در اروپا تا حدودی پیچیده کرده است.
شیمی سزیم در خاکها:
سزیم در خاک بواسطه ویژه گیهای جذب سطحی غالب است. استانتون و دیگران (Staunton et al) در سال 2002 گزارش نمودند که ویژه گیهای جذب سطحی خاک تا حدود بسیار زیادی بستگی به ترکیبات مواد معدنی شناخته (mineralogical) موجود در خاکها ذارد.
این وضعیت بخاطر آن است که مواد معدنی گل و لای مخصوصاً در غلظت های بسیار کم سزیم را بصورت انتخابی جذب می کنند.
این مسئله در واقع آلودگی رادیو سزیم را نسبت به سایر کاتیون ها از ارجحیت برخوردار کرده است.
مواد معدنی با بالاترین همخوانی برای مقدار نادر سزیم، میکاها(سنگ های معدنی نسوز) هیداراته یا الیت ها(رسوبات معدنی ثانویه یا سلکات های آلومینیومی لایه لایه) هستند.
برای مثال: ضریب انتخابی جینز – توماس .(Gaines – Thomas) در خصوص Cs – Ca محدود کننده ضریب برای رسوبات معدنی ثانویه ،کمتر از 1010 گزارش شده است.
در صورتیکه ضریب فوق برای Cs – Na در مراتب پائین تری قرار دارد، این ضرایب در حدود 105 و 102 گزارش شده اند.
اوزان Kd در حدود 105 برای الیت ها و 103 برای مونت موری لونت (Mont Moril Lonite) بیان شده است.
هنگامیکه سزیم در کناره سایت ها سائیده شده مبادله می گردد افتادگی بخشی از لایه بوجود می آید. بدین ترتیب هیدارسیون سزیم گرفته می شود. سوی نی (Sawhney) 1972.
کاهش فضای درون لایه ئی ممتد هنگامی که کاتیون قابل مبادله توسط مقادیری از سزیم پایدار که می تواند با استفاده ار دی فراکسیون Xr اندازه گیری شود، جایگزین می گردد. (X-ray diffraction)
کناره های سائیده شده با استفاده از میکروسکوپ (microscopy) نیز قابل رویت است.
بدین ترتیب جذب سطحی سزیم می تواند شکل ذرات و دانسیته لبه های سائیده شده ،مرتبط باشد.
راجک و دیگران (Rajec & et al) در سال 1999.
سزیم پایدار در سایت های کناری و حتی در سایت های درون لایه ئی میکا نیز شناسائی شده است. مک کین لی و دیگران (Mc Kinley & et al) در سال 2004.
به هر حال چندین مطالعه در خصوص فروپاشی (Collapse) لایه در حضور مقادیر کمی از رادیوسزیم صورت گرفته است و تا بحال محدودیت های آنا لی تیکی (آنالیز) مطالعات گسترده تری را غیر ممکن ساخته است. لی یو و دیگران (Liu & et al) در سال 2003.
با انجام آنالیز ها توسط سنسورهای میکرو Xr ثابت شد که سزیم 137Cs در کناره های میکا و کانال های داخلی با استفاده از انتشار در حالت جذب سطحی، تجمیع می گردد.
اوزان Kd برای خاکها ممکن است در خاکهای ماسه ئی یا خاکهای با محتوای ارگانیک بالا بزرگتر از اعدادی باشد که برای ایلیت (illite) خالص و بسیار کمتر برای مونت موری لونت (Mont Moril Lonite) گزارش شده است.
واترز و دیگران (Wauters & et al) در سال 1996 و اسمولدرز و دیگران (Smolders & et al) در سال 1997.
گفتگو های زیادی صورت گرفته است که ایلیت (illite) حتی به مقدار غیر قابل تشخیص در تعیین میزان جذب سطحی سزیم در خاکها بسیار مهم است.
البته بااستفاده از انالیز رگریسیون (regression analysis) امکان رسیدگی به این ادعا غیز محتمل است . هیرد و دیگران (Hird et al) در سال 1995.
این وضعیت ممکن است موردی برای اکثر خاکهائی باشد که در اقلیم های مختلف یعنی جائیکه ایلیت ها وجود دارند، باشد.
اگر چه مقادیر متفاوت است ولی به نظر نمی رسد موردی در خاکهای حاره ئی باشند. محققاً درجه فرسایش آب و هوا بر یکنواختی مواد معدنی خاک برای سزیم تاثیر می گذارد.
این موضوع تا کنون بنحو گسترده ئی مورد مطالعه قرار نگر فته است. به نظر می رسد که گل و لای خاک بیشتر از گل و لای مواد معدنی تحت فرسایش قرار می گیرند و بدین ترتیب یکنواختی بیشماری برای سزیم دارند.
برای مثال: استانتون و ل واسیس (Staunton & levacic) در سال 1999 گزارش کردند که اوزان Kd سزیم در فراکسیون خاکهای مختلف با اندازه گل و لای بزرگتر از ایلیت ها هستند.
این موضوع بدون توجه به تعیین مواد معدنی شناختی گل و لای با دی فراکسیون اشعه ایکس قابل اندازه گیری است
.( X-ray diffraction)
دومات و دیگران (Dumat & et al) در سال 1997 جذب سطحی سزیم را روی گل و لای مستخرجه از خاک خورد شده و خاک رویه بعد از حذف مواد ارگانیک، مقایسه کردند و بدین نتیجه رسیدند که جذب سطحی سزیم در خاک رویه در معرض فرسایش بیشتری قرار دارد و این موضوع بخاطر تغییرات اقلیمی و فعالیت بیولوژیکی است.
میس و دیگران (Maes & et al) در سال 1998 گزارش کردند که اثر کمپلکسیون فرسایش آب و هوا، بر تثبیت سزیم آشکار است. انها با مقایسه نمونه هائی از لایه های مختلف یک خاک این موضوع را اثبات کردند.
طبیعت فرسایش بادی و مطعاقباً اثر آن بر ویژه گیهای تثبیت سزیم بستگی به محتوای ارگانیک خاک دارد.
در لایه های مواد معدنی خاک پلی مرهای آلومینیوم سایت های فرسوده را سد کرده و از فرو رفتگی و متلاشی شدن لایه خاک جلوگیری می کند.
بدین ترتیب این گونه سایت ها انتخاب مستحکمی برای سزیم نمی باشند، در عوض در لایه های ارگانیک، آلومینیوم با لیگاندهای (Ligands) ارگانیک تشکیل کمپلکس می دهد.
لذا در چنین حالتی هنگامیکه سزیم هیدارته به شکل ضعیفی جذب سطحی شود، ضایعات در معرض فرورفتگی و متلاشی شدن (Collapse) قرار می گیرند.
دانشمندان فوق نیز ثابت کردند که فرسایش آب و هوائی ایجاد شده بصورت شیمیائی تحت شرایط کنترل شده جذب سطحی، سزیم را تغییر داده و ویژه گیهای تثبیت با توجه به سزیم نیز در این موضوع دخالت دارند.
میس و دیگران (Maes & et al) در سال 1999 و لی یو و دیگران (Liu & et al) در سال 2003 نشان دادند که مواد معدنی ثانویه رسوب داده شده روی ذرات میکائی (micaeous) نیز بصورت بسیار مستحکمی در جذب سطحی سزیم 137 (137Cs) دخالت دارند.
این مواد معدنی را می شود با استفاده از اوگزالات آمونیوم اسیدی شده حذف کرد. (acidified ammonium oxalate)
با پیشنهاد اینکه آنها شامل اکسیدهای آهن و سیلیکات های آلومینیوم هستند، با فرض اینکه جذب سطحی سزیم روی مواد ارگانیک غیر انتخابی است.
در چنین حالتی هیچگونه اثری از محتوای مواد ارگانیک خاک و جذب سطحی سزیم انتظار نمی رود.
اطلاعات جمع آوری شده در مکان های طبیعی یک همبستگی معکوس ، بین محتوای مواد ارگانیک خاک و بی تحرک سازی سزیم را نشان می دهد. وان برچیک (Van Bergeijk) در سال 1992 و ری گل و دیگران (Rigol et al) در سال 2002.
این مسئله به غیبت مواد معدنی گل و لای (خاک رس) در چنین خاکهائی نسبت داده شده است.
در هر صورت همانگونه که در بالا توضیح دادیم وجود مقادیر کمی از ایلیت ها می تواند یکنواختی بیشتری را فراهم نماید.
هم اکنون پذیرفته شده است که مواد ارگانیک اثر غیر مستقیمی بر جذب سطحی سزیم روی مواد معدنی خاک رس دارد. استانتون و دیگران (Staunton et al) در سال 2002.
اضافه شدن مولکولهای بزرگ ارگانیک (Organic Macromolecules) به مواد معدنی خاک رس منجر به کاهش در جذب سطحی سزیم می شوند.
این موضوع برای مواد هوموسی (humic) نیز صادق است. استانتون و روبوت (Staunton and Roubaud) در سال 1997 و دومات و استانتون (Dumat and Staunton) در سال 1999.
مواد ارگانیک خاک که با آب عصاره گیری شده است، پلی ساکاریدهای خاک و یک پروتئین نیز شامل مورد فوق هستند. دومات و دیگران(Dumat et al) در سال 2000.
اثر برای ایلیت بزرگتر از مونت موری لونیت (Mont morillonite) است.
سزیم در غلظت های ناچیز برجسته تر از غلظت های بالاتر است. این مشاهدات پیشنهاد می کند که جذب سطحی پلی مر نزدیک کناره سائیده های ایلیت(رسوبات معدنی ثانویه) مسئول این اثر است.
نتایج مشابه نیز با استفاده از نگرش های متضاد بدست آمده است. از قبیل حذف پیشرفته مواد ارگانیک خاک با استفاده از روشهای شیمیائی و فیزیکی.
دومات و دیگران(Dumat et al) در سال 1997 و استانتون و دیگران ( Staunton et al ) در سال 2000 حذف فیزیکی مواد ارگانیک خاک با استفاده از پلاسما اکسیژن سرد (Cold Oxygen plasma) ،نسبت به حذف شیمیائی اثر کمتری داشته است.
این موضوع بخاطر آن است که مواد ارگانیک روی سطوح قابل دسترس فیزیکی حذف می گردد. که ممکن است نقش مهمی در جذب سطحی سزیم و فرورفتگی لایه خاک نداشته باشند.
بعلاوه اهمیت مواد معدنی شناختی خاک ، خاک مواد ارگانیک ، ترکیب محلول و تبادل کمپلکس(ترکیب) مهم تلقی می گردند.
از آنجائیکه جذب سطحی رادیو سزیم یک فرآیند تبادلی است، طبیعت سایر کاتیون های رقابت کننده قابل چشم پوشی است.
سایت های تعادلی یکسانی که میل ترکیبی قوی برای سزیم دارند نیز کاتیون های مشابه را جذب می کنند.
کاتیون های مشابه از قبیل پتاسیم و آمونیوم بصورت انتخابی جذب می شوند. (بصورت گزینشی)
بدین ترتیب هنگامیکه مقدار زیادی از کمپلکس تبادلی با پتاسیم اشباع می شود، خاک میل ترکیبی کمتری با سزیم دارد.
بعلاوه پتاسیم در محلول بطرز موثری با سزیم در ارتباط با جذب سطحی، رقابت می کند و بنابراین امر جذب سطحی را کاهش می دهد.
این بررسی ها مفاهیم مهمی برای تغییر فصلی جابجائی سزیم محسوب می شود.
برای مثال: در طی رشد گیاه ممکن است ریزوسفر در پتاسیم حل شود و تا درجه معینی از تحلیل رفتن، کمپلکس تعادلی محلول را مجدداً بازسازی می کند.
شارژ سایت ها با میل ترکیبی بالا توسط پتاسیم جبران می شود.
در هر صورت هنگامیکه جریان تحلیل رفتن سزیم در محلول خاک و کمپلکس تبادلی در پتاسیم شدید باشد جذب سطحی سزیم افزایش می یابد. اسمولدرز و دیگران (Smolders et al) در سال 1997.
بر عکس تحت شرایط بدون اکسیژن از قبیل خاک های اشباع شده با آب، تولید آلومینیوم و محلول اکسید آهن می تواند منجر به جابجائی حرکت سزیم جذب سطحی شده باشد.
ایوانس و دیگران(Evans et al)در سال 1983و کمانس و دیگران(Comans et al) در سال 1989.
در مقابل با اثر کاتیون های مشابه، PH اثر مستقیمی بر جابجائی سزیم در خاکهای نواحی معتدل و رسوبات حاوی ایلیت، ندارد.
ممکن است همبستگی های قابل ملاحظه آماری بین PH خاک و جذب سطحی سزیم وجود داشته باشد. سانچیز و دیگران (Sanches et aj) در سال 2002.
ولی این همبستگی ها جدی نیست و معمولاً از فاکتورهای دیگری مثل محتوای مواد ارگانیک ناشی می گردد و ممکن است اثرات دراز مدت PH بر فرسایش مواد معدنی و جذب سطحی سزیم اثر بگذارد ولی چنین اطلاعاتی وجود ندارد.
جذب سطحی سزیم بر خاکها و خاکهای رس بنحو شدیدی وابسته به غلظت است.
بدین ترتیب اطلاعات بدست آمده با استفاده از غلظت های زیاد سزیم، مخصوصاً سزیم پایدار نمی تواند به غلظت های که معمولاً در محیط زیست وجود دارد، تعمیم داده شود.
وابستگی به غلظت بواسطه سطوح جذبی چندگانه ایست که سایت های با میل ترکیبی متفاوت برای سزیم دارند. بروور و دیگران (Brower et al) در سال 1983.
سزیم در غلظت های ناچیز فقط در سایت های با لبه های سائیده میل ترکیبی بالا، جذب سطحی می شود.
با افزایش غلظت سزیم تناسب میل ترکیبی پائین یا تبادل منظم سایت ها افزایش می یابد.
میل ترکیبی کلی و روی هم رفته سطح ،غالباً توسط کاهش های مقادیر (مقدار) Kb تعیین میگردد.
دانشمندان زیادی ارتباطات تدریجی بین ضرایب گزینشی و غلظت را مناسب می دانند.
بدین طریق آنها ضرایب میل ترکیبی با فراوانی نسبی را برای هر دو یا سه طبقه سایت های جذب سطحی که تعریف کرده اند بدست می آورند. بروور و دیگران (Brower et al) در سال 1983 و پونسوت و دیگران (Poinssot et al) در سال 1999.
در هر حال محاسبه دقیق این چنین پارامترهائی (4 یا 6) نیازمند نکات آزمایشی بیشتری می باشند.
یک تخمین احتیاطی تر، چند وجهی بودن سطح بوسیله اوزان گرادیان انتقال لوگاریتمی جذب سطحی فرینوند لیج
(Log – Transformed Frenundlich adsorption) معین میگردد.
این گرادیان اتحادی است برای ایزوترم های جذب سطحی خطی، هر اندازه گرادیان کوچکتر باشد وابستگی غلظت بزرگتر و سطح نسبت به جذب سطحی سزیم چند وجهی تر خواهد بود. اس پوزی تو (Sposito) در سال 1984این موضوع را گزارش کرد.
دانشمندان زیادی از قبیل:
Staunton and co – workers (Staunton 1994 Staunton and Roubaud 1997, Staunton and Levacic 1999) have reported values of about 0.5 to 0.6 for soils and soil clays, with little difference between soils contrastin
اوزانی در حدود 0.5 تا 0.6 برای خاکها و خاکهای رس، خاک با تفاوت های بسیار کمی بین خاکهای با مواد معدنی کانتراست گزارش کرده اند.
در صورتیکه کانتراست برجسته بین خاک رس های مرجع برای الیت 0.5 و برای مونت موری لونیت 0.8 مشاهده شده است.
خصوصیت دیگر سزیم که به طرز گسترده ئی مورد مطالعه قرار گرفته است دینامیک سزیم و تثبیت آن در طول زمان و سالمندی(پیر شدن) آن است.
مطالعات میدانی در خصوص دست یابی سزیم (bioavailability) نشان دادند که سزیم در طول سالهای متعاقب آلودگی، کاهش می یابد. وان برجیک (Vanbergeijk) 1992.
این موضوع به انتقال کند سزیم جذب سطحی شده به اشکالی که به سهولت مبادله نمی شوند یا اشکالی که سهولت مبادله آن کمتر است نسبت داده شده است.
احتمالاً به دلیل انتشار کند حالت جامد به محل های درون لایه ئی خاک رس داخلی یا از محل های خارجی به کناره سائیده شده داخلی در ایلیت باشد.
کمانس و دیگران (Comans et al) در سال 1991.
در هر صورت مطالعات آزمایشگاهی و مدلینگ پدیده فوق را بنحوی که قادر باشند مشاهدات میدانی را تشریح نماید، تولید نکرده اند.
جذب سطحی تا حدود زیادی سریع بوده و برای تبادل کاتیونی با مقدار بسیار کمی واکنش مداوم انجام می گردد.
تعیین عدم جذبیت (جذب شدن) سزیم بسیار مشکل است و مطالعات زیادی شرایط معینی را برای جذب سطحی و عدم آن مورد استفاده قرار نمی دهد.
لذا جذب سطحی قوی یا جذب سطحی غیر قابل برگشت اشباع می شود.
گوئی وارچ و دیگران (Guivarch et al) در سال 1999 به این نتیجه رسیده اند که اوزان Kd واحدی برای سزیم بین 2 تا 6 بار بزرگتر از اوزان Kd جذب سطحی آن است.
این موضوع به غلظت سزیم پایدار بستگی داشته و مطابق با بین 50 و 80 درصد سزیم جذب سطحی شده ، تثبیت شده است. (سزیمی که به سهولت دچار واجذبی نمی شود)
در هر صورت دانشمندان هیج تلاشی برای دنبال کردن تغییرات در تثبیت سزیم با زمان انجام نداده اند.
دی کونینگ و کمانس (de koning & comans) در سال 2004 نشان دادند که بین 44 و 91 درصد جذب سطحی سزیم در ایلیت فوراً برگشت پذیر نیست و بستگی به کاتیون اشباع کننده دارد.
ایجاد یک روند با زمان با توجه به دلالت کم تثبیت اولیه، بسیار مشکل است. اگر چه ممکن است تا حدودی تثبیت وابسته به زمان وجود داشته باشد.
پدیده پیری سزیم محقیقاً نیز بدلیل تغییرات در توزیع سزیم در خاک متراکم بعد از توزیع یکنواخت آن در سطح است.
این پدیده در برگیرنده نفوذ سزیم به داخل مشتقات خاک و حرکت آهسته ی آن رو به پائین در پروفایل خاک می باشد.
مطالعات مدلینگ نشان داده است که چگونگی جذب سزیم در ریشه ها بستگی به پروفیل های نسبی ریشه ها دارد.
عمق خاک براحتی آلاینده سزیم را جذب ریشه های عمقی گیاهان می نماید. دارا و استانتون (Darrah & Staunton) در سال 2000.
ریشه های گیاهان سزیم را براحتی جذب می کنند و این موضوع بخاطر شباهت سزیم با ماده مغذی ضروری یعنی پتاسیم است.
گیاهان در تجمع سزیم متفاوتند . برادلی و وایلی (Broadly & Willey) در سال 1997.
این تفاوت در واقع بدلیل تفاوتها در الگوی ریشه ئی شدن جذب ریشه ئی یا جابجائی شدن (Translocation) درون گیاه است. ولی این علت بصورت شفافی شناسائی نشده است.
سزیم در درون گیاهان قابلیت جابجائی داشته و روندهای شدید جابجائی و جایگیری درون گیاهان با پتاسیم را دارد.(روند جابجائی سزیم در گیاهان شبه پتاسیم است)
برادلی و وایلی (Broadly & Willey) در سال 1997 و اسمولدرز (Somolders) در سال 2000.
اطلاعات نسبتاً کمی در خصوص تفاوتهای بین گونه ها در ظرفیت شان برای تمایز بین سزیم و پتاسیم وجود دارد به نظر می رسد که آستانه جذب سزیم توسط ریشه ها با کاهش غلظت پتاسیم افزایش یابد.
مقدار این آستانه، عددی در حدود یک مول بر لیتر (1 mmol L-1)، 250 میکرومول بر لیتر (250 µ mol L-1) یا 20 میکرومول بر لیتر (µmol L-1 20)گزارش شده است. زو (Zhu) و سایر دانشمندان در سال 2001 .
این بازدارندگی ممکن است حد اقل بخشی از آن به علت جریان افزایش یافته سزیم جذب شده، باشد.
زو و دیگران (Zhu et al) در سال 1999 پیش گوئی های مدلینگ مربوط به جذب سزیم ،غالبا فرآیند جذب را بالاتر از اوزان واقعی پیش گوئی کردند.
اگر غلظت خاک محلول پتاسیم زیر یک mm باشد پیش گوئی ها بهبود می یابد. والگو – کالزادا (Vallego – Calzada) در سال 2000.
مشخص گردیده است که جذب سزیم در تنگنای پتاسیم (Staruaiton) افزایش می یابد. جونز و دیگران در سال 1998، برادلی و دیگران در سال 1999b، زو و دیگران در سال 2000. (Jones et al, Broadly et al, Zhu et al)
ولی این اثر کوتاه مدت است. وایلی و مارتین در سال 1997 و استانتون و دیگران در سال 2003(Willey & Martin, Staunton et al) به نتیجه فوق رسیده بودند.
اگر چه اغلب گیاهان در سیستم های طبیعی و کشاورزی با می کوریزا (Mycorihiza) که همراه با آب و مواد غذائی وارد آنها می شود، آلوده می گردند ولی اطلاعات خیلی محدودی در خصوص اثر عفونت می کوریزائی (Mycorihizal infection) در جذب وجابجائی سزیم وجود دارد.
دریسنر و دیگران(Drissner et al) در سال 1998و روسن و دیگران(Rosen et al) در سال 2005 گزارش کردند که قارچ می کوریزائی آربیوس کیولار (Arbuscular Mycorahiza Fungus) جذب سزیم را توسط تره فرنگی (Leek) افزایش می دهد. ولی اثری بر علف های چاودار (گندم سیاه) ندارد.
البته آنها نتوانسته اند بطور قطع اثبات کنند که آیا نبود یک اثر مشاهده شده برای علف های گندم بدلیل عفونت ضعیف یا تراکم ریشه های زیاد می باشد.
در مقابل ریسن و برونر (Riesen & Brunner) در سال 1996 پیدا کردند که عفونت اکتومیوکورزالی(ectomyocorrhizal) جذب سزیم را کاهش داده است.
دی کلرک و دیگران (Declerck et al) در سال 1996 نشان دادند که می کوریزا (Mycorihiza) می تواند رادیو سزیم را جذب کرده و انتقال دهد و احتمالاً آنرا تجمیع نماید.
بعداً همان گروه نشان دادند که جذب رادیو سزیم برای هیفای می کوریزائی (Mycorihizai hyphae) نسبت به ریشه ها کمتر و پائین تر است.
دی بولوس و دیگران (De Boulois etal) در سال 2005 نیز توجه دادند که ساختارهای قارچی درون رادیکالی
intraradical fungal structures)) مقداری تجمع محلی سزیم را میسر می سازد. بدین ترتیب کاهش جابجائی درون ریشه ها بوجود می آید.
در عوض کلینت و دیگتون (Clint & Dighton) در سال 1992 نتیجه گیری کردند که علی رغم پائین بودن کلیت جذب از خاک عفونت می کوریزا (Mycorihiza) منجر به افزایش جابجائی و انتقال سزیم به طرف ساقه ها و شاخه ها می گردد.
قطعاً، اثر عفونت می کوریزا (Mycorihiza) بر جذب و جابجائی رادیو سزیم از خاک متغیر بوده و بستگی به خاک و قارچ (همخانه میزبان) دارد.
البته لازم است که تحقیقات بیشتری روی این موضوع صورت پذیرد.
اطلاعات نسبتاً بیشتری در خصوص جذب سزیم توسط اجسام میوه ئی قارچ، مخصوصاً قارچ های خوراکی وجود دارد.
کاملاً مشخص است که مصرف قارچ های رشد داده شده روی خاکهای آلوده توسط حیوانات و انسان طریقه بسیار مهمی برای ورود سزیم به زنجیره غذائی است.
بارنت و دیگران (Barneit et al) در سال 1999 و باضا و دیگران (Baeza et al) در سال 2005 اعلام کردند که سزیم موجود در قارچ براحتی قابل هضم است. باضاء و گولن (Baeza & Guillen) .
انتقال سزیم ازخاک به قارچ کاملاً متغیر است و روند مشخصی در خصوص اینکه چه فاکتورهای تفاوتها را بوجود می آورند توسط گلت و کوروت (Gillet & Crout) در سال 2000 بیان گردیده است.
قارچ های غیر قابل خوراکی نیز سزیم را در خود تجمیع می نمایند و ممکن است این مسئله نه فقط بر گونه سزیم تاثیر داشته باشد بلکه نیز منجر به توضیح مجدد آن در خاک می شود. شاند و دیگران (Shand etal) در سال 1995 و آندرسون و دیگران (Anderson et al) در سال 1997.
اطلاعات کمی در خصوص نقش مستقیم و یا غیر مستقیم و یا باکتری خاک بر دینامیک سزیم وجود دارد.
روسل و دیگران (Russel et al) در سال 2004 گزارش کردند که باکتری های کاهنده سولفات
(bacterial sulfate reduction) جذب سزیم را در خاک های خشک و حاره ئی کاهش می دهد.
ولی آنها مکانیزم مشخصی برای این ادعا ارائه ندادند.
به نظر نمی رسد که تجمع سزیم ،میکروارگانیسم های خاک را بعنوان یک انبار ذخیره مهم برای سزیم غیر متحرک در خاک های معدنی، مورد استفاده قرار دهد.
این موضوع بخاطر آن است که جذب سطحی سزیم در خاک های رسی به مراتب بیشتر از سایر خاکهاست.
در هر حالتی موضوع فوق در خاک های ارگانیک یافت نمی شود. سانچیز و دیگران (Sanches et al) در سال 2000.
و نکته پایانی اینکه،آلودگی خاک با مواد رادیو اکتیو اثرات دراز مدت،مهلک و مرگ اوری را بر همه موجودات زنده محیط زیست و در راس آنها، انسان تحمیل میکند وبدین ترتیب لازم است دولت ها و ملت ها برای پیش گیری از الودگی خاک عزیز با مواد رادیو اکتیو،نهایت سعی و تلاش را در دستور فعالیت های پیشگیرانه داشته باشند.همه باید بدانیم که سلامت انسان و سایر سامانه های حیات وابستگی تام به سلامت خاک دارد.

ایام به کام/22/دی ماه/1395 شرکت معظم پارس خودرو-دکتر سلطانی نژاد.


